题目内容
17.已知NH4CuSO3与足量的5mol•L-1硫酸溶液混合微热,产生下列现象::①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色.据此判断下列说法正确的是( )| A. | 反应中硫酸作氧化剂 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 刺激性气味的气体是氨气 | |
| D. | 1mol NH4CuSO3完全反应转移0.5mol电子 |
分析 NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,则NH4CuSO3中Cu的化合价为+1价,以此解答该题.
解答 解:反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+.
A、由发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,反应只有Cu元素的化合价发生变化,硫酸根反应前后未变,反应中硫酸体现酸性,不作氧化剂,故A错误;
B、NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,反应前后S元素的化合价没有发生变化,故B错误;
C、因反应是在酸性条件下进行,不可能生成氨气,故C错误.
D、反应只有Cu元素的化合价发生变化,分别由+1→+2,+1→0,反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,每2molNH4CuSO3参加反应则转移1mol电子,则1molNH4CuSO3完全反应转移0.5mol电子,故D正确;
故选D.
点评 本题考查氧化还原反应,难度较大,注意从反应现象判断生成物,结合化合价的变化计算电子转移的数目.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
9.下列说法正确的是( )
| A. | pH<7的溶液一定是酸性溶液 | |
| B. | 室温时pH=5的溶液和pH=3的相比,前者c(OH-)是后者的100倍 | |
| C. | 室温下,每1×107个水分子中只有一个水分子发生电离 | |
| D. | HCl溶液中无OH-,NaCl溶液中既无OH-也无H+ |
10.为使Na2S溶液中$\frac{c(N{a}^{+})}{c(H{S}^{-})}$的值减小,可加入的物质是( )
①适量的盐酸;②适量的NaOH溶液;③适量的KOH溶液;④适量的KHS溶液.
①适量的盐酸;②适量的NaOH溶液;③适量的KOH溶液;④适量的KHS溶液.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
5.在水溶液里或熔融状态下能导电的化合物是电解质.下列物质不属于电解质的是( )
| A. | Cu | B. | NaOH | C. | H2SO4 | D. | Na2SO4 |
12.下列各组粒子在指定的溶液中能大量共存的是( )
| A. | 加入铝片能放出氢气的溶液:Na+、CO32-、NO3-、NH4+ | |
| B. | 滴入酚酞显红色的溶液:CO32-、Na+、AlO2-、NO3- | |
| C. | 能使蓝色石蕊试纸变红的溶液:Na+、Cl-、S2-、ClO- | |
| D. | 滴入甲基橙显红色的溶液:MnO4-、K+、SO42-、CH3CH2OH |
9.将agFe2O3、Al2O3样品溶解在过量的200mL浓度为0.1mol•L-1的盐酸溶液中,然后向其中加入NaOH溶液,使Al3+、Fe3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
| A. | 0.1 mol/L | B. | 0.2 mol/L | C. | 0.4 mol/L | D. | 0.6mol/L |
6.下列说法中正确的是( )
| A. | 氧化还原反应的实质是相互交换成分 | |
| B. | 在氧化还原反应中,化合价变化的一定是不同元素 | |
| C. | 在氧化还原反应中,氧化剂与还原剂一定是不同物质 | |
| D. | 某元素由游离态转化为化合态,这种元素不一定被氧化了 |
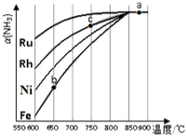 氨气在生产、生活和科研中应用十分广泛.
氨气在生产、生活和科研中应用十分广泛.