题目内容
下列反应的离子方程式书写正确的是( )
| A、氧化铜与稀硫酸反应:CuO+2H+═Cu2++H2O |
| B、碳酸钙和稀盐酸反应:2H++CO32-═CO2↑+H2O |
| C、氯气和氯化亚铁溶液反应:Cl2+Fe2+═Fe3++2Cl- |
| D、铜和浓硝酸反应:Cu+2H+═Cu2++H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、氧化铜为氧化物书写离子方程时应写化学式;
B、碳酸钙不溶于水,离子方程式中应写成化学式;
C、得失电子不守恒导致电荷不守恒;
D、不符合客观事实,应铜和浓硝酸中+5价的氮元素发生的氧化还原反应.
B、碳酸钙不溶于水,离子方程式中应写成化学式;
C、得失电子不守恒导致电荷不守恒;
D、不符合客观事实,应铜和浓硝酸中+5价的氮元素发生的氧化还原反应.
解答:
解:A、氧化铜为氧化物书写离子方程时应写化学式,正确的离子方程式为CuO+2H+═Cu2++H2O,故A正确;
B、碳酸钙不溶于水,离子方程式中应写成化学式,正确的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,故B错误;
C、得失电子不守恒导致电荷不守恒,离子方程式为Cl2+2Fe2+═2Fe3++2Cl-,故C错误;
D、不符合客观事实,应铜和浓硝酸中+5价的氮元素发生的氧化还原反应,正确的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故D错误;
故选A.
B、碳酸钙不溶于水,离子方程式中应写成化学式,正确的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,故B错误;
C、得失电子不守恒导致电荷不守恒,离子方程式为Cl2+2Fe2+═2Fe3++2Cl-,故C错误;
D、不符合客观事实,应铜和浓硝酸中+5价的氮元素发生的氧化还原反应,正确的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故D错误;
故选A.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、得失电子守恒以及是否符合反应实际的角度分析.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
根据下列变化,判断属于还原反应的是( )
| A、HCl→Cl2 |
| B、S→SO2 |
| C、Fe(OH)3→Fe2O3 |
| D、CuO→Cu |
短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数相差8,A原子的最外层电子数是其次外层电子数的3倍,B单质的焰色反应为黄色.下列说法正确的是( )
| A、气态氢化物的热稳定性:A<C |
| B、元素A与B只能形成一种化合物 |
| C、最高价氧化物对应的水化物的酸性:C>D |
| D、原子半径的大小顺序:rB>rC>rD>rA |
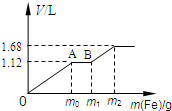 向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如右图所示,且每一段只对应一个反应.下列说法正确的是( )
向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如右图所示,且每一段只对应一个反应.下列说法正确的是( )| A、产生氢气的体积为1.68L |
| B、产生二氧化氮的体积为1.12L |
| C、参加反应铁粉的总质量m2=5.6g |
| D、原混合溶液中c(HNO3)=0.5 mol?L-1 |
下列过程中需要吸收热量的是( )
| A、H2→2H |
| B、2H2+O2═2H20 |
| C、CaO+H20=Ca(OH)2 |
| D、2Cl→Cl2 |
 向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中XZ的物质的量浓度随时间变化的曲线.
向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中XZ的物质的量浓度随时间变化的曲线.