题目内容
5.下列化学反应既属于氧化还原反应又属于四种基本反应类型的是( )| A. | Cu+2FeCl3═CuCl2+2FeCl2 | |
| B. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | |
| C. | Cl2+2KI═2KCl+I2 | |
| D. | 2CuSO4+2H2O $\frac{\underline{\;通电\;}}{\;}$2Cu+2H2SO4+O2↑ |
分析 含元素化合价变化的反应为氧化还原反应,结合四种基本反应类型来解答.
解答 解:A.Fe、Cu元素化合价发生变化,属于氧化还原反应,但不属于四种基本反应类型,故A不选;
B.不含元素的化合价变化,为非氧化还原反应,故B不选;
C.Cl、I元素化合价发生变化,属于氧化还原反应,且属于置换反应,故C选;
D.Cu、O元素化合价发生变化,属于氧化还原反应,但不属于四种基本反应类型,故D不选.
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应判断方法,题目难度不大.

练习册系列答案
相关题目
15.下列说法不正确的是( )
| A. | 盐的组成中不一定含有金属元素 | |
| B. | 强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 | |
| C. | 同种元素在不同的化合物中的化合价不一定相同 | |
| D. | 由同种元素组成的物质一定是单质 |
13.向集满CO2的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起.上述实验过程中没有发生的离子反应是( )
| A. | Al3++4OH-→[Al(OH)4]- | B. | Al2O3+2OH-+3H2O=2[Al(OH)4]- | ||
| C. | CO2+2OH-=CO32-+H2O | D. | 2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ |
20.关于下列各装置图的叙述中,正确的是( )
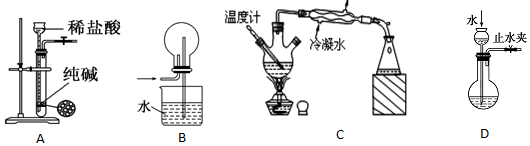

| A. | 用图A装置制取少量CO2气体 | |
| B. | 多余的NH3可用图B装置吸收 | |
| C. | 装置C可分离沸点不同且互溶的液体混合物 | |
| D. | 图D可检查装置的气密性 |
10.下列说法正确的是( )
| A. | CO和NO都是大气污染物,在空气中都能稳定存在 | |
| B. | Al在浓硫酸中会“钝化”能用铝槽盛放浓硫酸 | |
| C. | 四氯化碳常用作灭火剂 | |
| D. | 在碱性溶液中可以大量存在:S2O32-、AlO2-、SiO32-、S2-、Na+ |
17.溶液、胶体、浊液三种分散系最本质的区别是( )
| A. | 稳定性 | B. | 透明度 | ||
| C. | 能否发生丁达尔现象 | D. | 分散质微粒大小 |
14.下列说法中正确的是( )
| A. | 1molC质量是12 g•mol-1 | |
| B. | 22.4L H2的物质的量是1mol | |
| C. | 将60gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是1.5mol•L-1 | |
| D. | NaCl的摩尔质量是58.5 g•mol-1 |
 )的官能团的名称为碳碳双键、羟基.
)的官能团的名称为碳碳双键、羟基.