题目内容
14. 2009年10月15日新华社报道:全国农村应当在“绿色生态•美丽多彩•低碳节能•循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题:
2009年10月15日新华社报道:全国农村应当在“绿色生态•美丽多彩•低碳节能•循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题:(1).煤的气化和液化可以提高燃料的利用率.
已知25℃、101kPa时:
①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-126.4kJ/mol
②2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol
③H2O(g)═H2O(l)△H=-44kJ/mol
则在25℃、101kPa时:C(s)+H2O(g)═CO(g)+H2(g)△H=+115.4kJ•mol-1.
(2).高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)?Fe(s)+CO2(g)△H>0
已知在1 100℃时,该反应的化学平衡常数K=0.263.
①该反应的化学平衡常数表达式为$\frac{c(C{O}_{2})}{c(CO)}$
温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值增大(填“增大”“减小”或“不变”).
②1 100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?否(填“是”或“否”),反应向因为Qc=$\frac{c(C{O}_{2})}{c(CO)}$=0.25<K=0.263(填“正”或“逆”) 方向进行.
(3).目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.
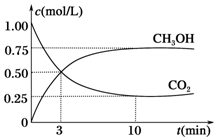
现向体积为1L的容积固定的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)=0.225mol/(L•min).
②下列措施能使$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$ 增大的是BD(填字母).
A.升高温度 B.再充入H2 C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大 F.若维持容器内压强不变,充入He(g)
(4)有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染.请你判断是否可行并说出理由否,该反应是一个焓增、熵减的反应,任何情况下不能自发进行.
分析 (1)依据化学方程式和盖斯定律计算得到;
(2)①平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$;反应是吸热反应,温度升高平衡正向进行,平衡常数增大;
②依据浓度商和平衡常数比较判断平衡移动的方向;
(3)①依据图象分析,达到平衡时物质的浓度变化,结合反应速率概念计算得到;
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.依据平衡移动方向分析判断$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$变化;
A.升高温度平衡逆向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$减小;
B.再充入H2 平衡正向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$增大;
C.再充入CO2 平衡正向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$减小;
D.将H2O(g)从体系中分离平衡正向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$增大;
E.充入He(g),使体系压强增大,分压不变,平衡不动,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$不变;
(4)根据△G的大小判断反应能否进行.
解答 解:(1)①C(s)+1/2O2(g)=CO(g)△H=-126.4kJ•mol-1
②2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ•mol-1
③H2O(g)=H2O(l)△H=-44kJ•mol-1
依据盖斯定律①-$\frac{②}{2}$+③得到C(s)+H2O(g)=CO(g)+H2(g)△H=+115.4 kJ•mol-1;
则在25℃,101kPa时:C(s)+H2O(g)=CO(g)+H2(g)△H=+115.4 kJ•mol-1;
故答案为:+115.4 kJ•mol-1;
(2)①FeO(s)+CO(g)?Fe(s)+CO2(g),反应的平衡常数K=$\frac{c(C{O}_{2})}{c(CO)}$,FeO(s)+CO(g)=Fe(s)+CO2(g)△H>0,温度升高,化学平衡移动后达到新的平衡,平衡正向进行,平衡常数增大,
故答案为:$\frac{c(C{O}_{2})}{c(CO)}$;增大;
②1100℃时测得高炉中,c(CO2)=0.025mol•L-1,c(CO)=0.1mol•L-1,则在这种情况下,Qc=$\frac{c(C{O}_{2})}{c(CO)}$=$\frac{0.025mol/L}{0.1mol/L}$=0.25<K=0.263;反应未达到平衡,正向进行,
故答案为:否;因为Qc=$\frac{c(C{O}_{2})}{c(CO)}$=0.25<K=0.263;
(3)①②CO2(g)+3H2(g)?CH3OH(g)+H2O(g),依据图象分析达到平衡后,c(CH3OH)=0.75mol/L,c(CO2)=0.25mol/L,反应消耗的氢气浓度c(H2)=2.25mol/L,氢气的平均反应速率v(H2)=$\frac{2.25mol/L}{10min}$=0.225 mol/(L•min),
故答案为:0.225 mol/(L•min);
③CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.依据平衡移动方向分析判断$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$变化;
A.升高温度平衡逆向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$减小;
B.再充入H2 平衡正向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$增大;
C.再充入CO2 平衡正向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$减小;
D.将H2O(g)从体系中分离平衡正向进行,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$增大;
E.充入He(g),使体系压强增大,分压不变,平衡不动,$\frac{c(C{H}_{3}OH)}{c(C{O}_{2})}$不变;
故答案为:BD;
(4)反应2CO=2C+O2(△H>0、△S<0),则△G=△H-T•△S>0,反应是一个焓增、熵减的反应,任何情况下不能自发进行;
故答案为:否,该反应是一个焓增、熵减的反应,任何情况下不能自发进行.
点评 本题考查了热化学方程式和盖斯定律的计算应用,平衡盘点和平衡常数的计算应用,反应速率图象分析判断,影响平衡因素的分析应用,题目难度中等.

 快捷英语周周练系列答案
快捷英语周周练系列答案 氯及其化合物在生产、生活中有广泛的用途.回答下列问题:
氯及其化合物在生产、生活中有广泛的用途.回答下列问题:(1)“氯氧化法”是指在碱性条件下用Cl2将废水中的CN-氧化成无毒物质.写出该反应的离子方程式:5Cl2+2CN-+8OH-═10Cl-+N2↑+2CO2↑+4H2O.
(2)地康法制备氯气的反应为4HCl(g)+O2(g)$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$2Cl2(g)+2H2O(g)△H=-115.6kJ•mol-1,1molH-Cl、1molCl-Cl、1molO-O断裂时分别需要吸收431J、243kJ、489kJ的能量,则1molO-H断裂时需吸收的能量为460.65kJ.
(3)取ClO2消毒过的自来水(假定ClO2全部转化为Cl-)30.00mL,在水样中加入几滴K2CrO4溶液作指示剂,用一定浓度AgNO3溶液滴定,当有砖红色的Ag2CrO4沉淀出现时,反应达到滴定终点,测得溶液中CrO42-的浓度是5.00×10-3mol•L-1,则滴定终点时溶液中c(Cl-)=8.90×10-6mol/L.[已知:Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12]
(4)在5个恒温、恒容密闭容器中分别充入4molClO2(g),发生反应:4ClO2)(g)?2Cl2O(g)+3O2(g)△H>0,测得ClO2(g)的部分平衡转化率如表所示.
| 容器编号 | 温度/ | 容器体积/L | ClO2(g)的平衡转化率 |
| a | T1 | V1=1L | 75% |
| b | T2 | V2 | |
| c | T3 | V3 | 75% |
| d | |||
| e |
①该反应中Cl2O是还原产物(填“还原产物”或“氧化产物”).
②T1℃时,上述反应的平衡常数K=25.63.
③V2>(填“>”、“<”或“=”)V3.
④d、c两容器中的反应与a容器中的反应均各有一个条件不同,a、d、e三容器中反应体系总压强随时间的变化如图所示,a、d、e三容器中ClO2的平衡转化率由大到小的排列顺序为e<a=d(用字母表示);与a容器相比,d容器中改变的一个实验条件是加入催化剂,其判断依据是ad图象中曲线变化可知,d反应速率增大,压强不变平衡点不变.
| A. | 氢气、天然气 | B. | 液化气、核能 | C. | 太阳能、风能 | D. | 燃煤、97#汽油 |
| A. | NaHCO3溶液:HCO3-+H2O?CO32-+H3O+ | |
| B. | NaHS溶液:HS-+H2O?H2S+OH- | |
| C. | 硫酸铝溶液跟碳酸氢钠溶液反应:Al3++3HCO3-+6H2O?Al(OH)3↓+3CO2↑ | |
| D. | NH4Cl溶于D2O中:NH4++D2O?NH3HDO+H+ |
| A. | Na+、NO3-、Cl- | B. | Cu2+、K+、NO3- | C. | H+、HCO3-、NO3- | D. | Na+、Ba2+、SO42- |
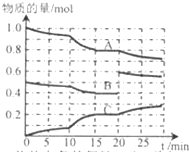 在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
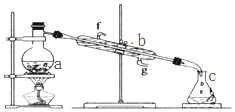 掌握仪器名称、组装及使用方法是中学化学实验的基础,图为蒸馏实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,图为蒸馏实验装置.