题目内容
1.设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )| A. | 1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 | |
| B. | 常温下,16gO2和O3的混合气体中含有的氧原子数为NA | |
| C. | 标准状况下,22.4 L NO 和22.4 L O2混合后所得气体中分子总数为1.5 NA | |
| D. | 将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5 NA |
分析 A.胶体粒子是氢氧化铁形成的集合体;
B.O2和O3均由氧原子构成;
C.一氧化氮与氧气反应生成二氧化氮,二氧化氮与四氧化二氮之间存在转化平衡,所以反应后的物质中含有的分子数减小;
D.氯气所处的状态不明确,因此物质的量不明.
解答 解:A.胶体粒子是氢氧化铁形成的集合体,1molFeCl3与沸水反应生成胶体后,Fe(OH)3胶粒小于NA个,故A错误;
B.O2和O3均由氧原子构成,16g混合物中含有的氧原子的物质的量n=$\frac{16g}{16g/mol}$=1mol,含有的氧原子数为NA,故B正确;
C.根据2NO+O2═2NO2可知:标准状况下,22.4 L NO即1molNO 和22.4 L O2 即1mol氧气混合后所得气体的物质的量为1.5mol,但由于NO2气体中存在平衡:2NO2?N2O4,导致分子总数小于1.5 NA,故C错误;
D.缺少温度和压强,无法确定11.2 LCl2的物质的量,无法确定转移的电子数,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的运用以及物质的状态和结构是解题关键,难度中等.

练习册系列答案
相关题目
11.表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )

| A. | 常压下五种元素的单质中,Z单质的沸点最高 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | W的氢化物比X的氢化物稳定 | |
| D. | Y元素最高价氧化物对应水化物比W元素的最高价氧化物对应水化物的酸性强 |
12.经测定某微粒有与H2S拥有相同的电子数,它不可能是( )
| A. | HCl | B. | HS- | C. | NH2- | D. | Ca2+ |
9.现将标准状况下的2.24L HCl气体溶解在含有0.2mol醋酸钠溶液的烧杯中,测得溶液体积为1L.若此溶液中c(CH3COO-)>c(Cl-),则下列判断中不正确的是( )
| A. | c(CH3COO-)+c(OH-)=0.10 mol•L-1 | B. | c(CH3COOH)+c(CH3COO-)=0.20 mol•L-1 | ||
| C. | c(CH3COOH)<c(CH3COO-) | D. | 温度为298 K时,pH<7 |
6.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 L 0.5 mol•L-1 Na2CO3溶液中含有的CO32-数目为0.5NA | |
| B. | 标准状况下,2.24 L C4H8含有的共用电子对数等于1.1NA | |
| C. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| D. | 27 g Al在标准状况下2.4 L Cl2中燃烧,转的2移的电子总数为3NA |
13.从柑橘中炼制的萜二烯其结构简式为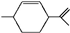 .有关萜二烯的说法不正确的是( )
.有关萜二烯的说法不正确的是( )
 .有关萜二烯的说法不正确的是( )
.有关萜二烯的说法不正确的是( )| A. | 萜二烯的分子式为C10H16,不属于芳香烃 | |
| B. | 可溶于乙醇或乙醚,不溶于水 | |
| C. | 萜二烯分子中所有碳原子处于同一个平面上 | |
| D. | 萜二烯与过量的溴的四氯化碳溶液反应后的产物为 |
11.据报道,铀是一种放射性元素,23592U是核电站的主要燃料.下列关于23592U的说法正确的是( )
| A. | 质量数为235 | B. | 质子数是235 | ||
| C. | 中子数为92 | D. | 与23892U是同种原子 |