题目内容
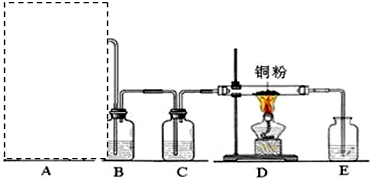
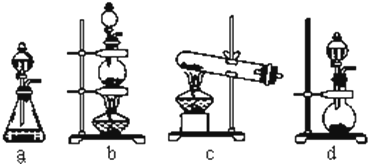
16.利用反应Zn+2FeCl3═ZnCl2+2FeCl2设计一个原电池.(1)在如图图方格内画出实验装置图,
(3)外电路中的电子是从负(Zn)极流向正(Pt或石墨)极.
分析 根据反应“Zn+2FeCl3═ZnCl2+2FeCl2”可知,反应中Zn被氧化,应为原电池负极,失电子而被氧化,
正极应为活泼性比Zn弱的金属或非金属材料,Fe3+在正极得到电子而被还原,电解质溶液为FeCl3,以此画出实验装置图并书写有关的电极反应式.
解答 解:(1)由反应“Zn+2FeCl3═ZnCl2+2FeCl2”可知,反应中Zn被氧化,应为原电池负极,失电子而被氧化,
正极应为活泼性比Zn弱的金属或非金属材料,Fe3+在正极得到电子而被还原,电解质溶液为FeCl3,实验装置图: ,
,
故答案为: ;
;
(2)正极为Pt(或石墨),三价铁离子在正极得电子发生还原反应,电极反应式为Fe3++e-=Fe2+,负极为活泼金属锌,失电子发生氧化反应,电极反应为Zn-2e-=Zn2+,故答案为:Pt(或石墨);Fe3++e-═Fe2+;Zn;氧化反应;
(3)原电池工作时,电子从负极流出,沿导线流向正极,故答案为:负(Zn);正(Pt或石墨).
点评 本题考查原电池的设计及原电池的工作原理,题目难度不大,注意从氧化还原反应的角度由电池反应判断电极反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.有些化学反应不仅与反应物种类有关,还与反应条件(反应温度、反应物浓度)或反应物物质的量的比值有关,下列反应中不随反应条件(反应温度、反应物浓度)、反应物物质的量的而变化的是( )
| A. | 氯气与铁粉 | B. | 二氧化碳与石灰水 | ||
| C. | 锌与硫酸 | D. | 碳酸钠与硫酸 |
8.下列说法正确的是( )
| A. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| B. | 将NH4Cl溶液蒸干制备NH4Cl固体 | |
| C. | 因为NH3能使酚酞溶液变红,NH3用于设计喷泉实验 | |
| D. | 浓氨水可检验氯气管道是否漏气 |
 锰及其化合物有广泛应用.
锰及其化合物有广泛应用.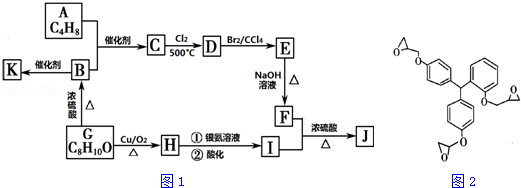
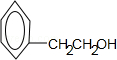 .
. ;F+I→J
;F+I→J .
.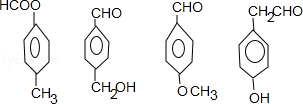 .
.
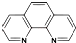 ),它能与Fe2+形成红色配合物(如图甲),该配离子中Fe2+与氮原子形成配位键共有6个.
),它能与Fe2+形成红色配合物(如图甲),该配离子中Fe2+与氮原子形成配位键共有6个.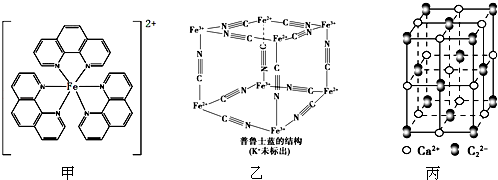
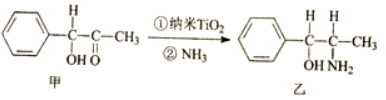
 ,其中σ键与π键数目之比为1:2.
,其中σ键与π键数目之比为1:2.