题目内容
9.下列叙述中能肯定说明金属A比金属B的活泼性强的是( )| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 将A、B组成原电池时,A为正极 | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 将A和B用导线相连接,一同放入CuSO4溶液中,B的表面有红色的铜析出 |
分析 判断金属性强弱的依据:元素原子的失电子能力、单质从酸(或水)中置换的H2的难易程度、最高价氧化物水化物的碱性强弱、原电池中的正负极等.
解答 解:A、金属性强弱和原子的最外层电子数无关,如氢原子最外层只有一个电子,而镁原子最外层两个电子,镁的金属性更强,故A错误;
B、形成原电池时,一般金属性强的作负极,故B错误;
C、金属性强弱取决于单质从酸(或水)中置换的H2的难易程度,和置换的H2多少无关,故C错误;
D、将A和B用导线相连接,一同放入CuSO4溶液中,B的表面有红色的铜析出,则B为正极,A为负极,负极比正极活泼,说明A的金属性比B强,故D正确.
故选D.
点评 本题考查学生判断金属性强弱的依据,熟悉金属性比较的常见方法即可解答,侧重于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
19.乙醇、乙二醇、丙三醇中分别加入足量金属钠,产生等体积的氢气(相同条件下),则上述三种醇的物质的量之比是( )
| A. | 3:2:1 | B. | 1:1:1 | C. | 1:2:3 | D. | 6:3:2 |
17.下列描述中不正确的是( )
| A. | CS2为直线形的非极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | SF6中有6对完全相同的成键电子对 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
4.日本福岛第一核电站发生严重的核辐射泄漏,日本政府向福岛核电站附近居民发放碘片(12753I),以降低放射性碘对人体的伤害.已知核辐射中放射性碘(碘13153I)的核电荷数为53,则下列说法正确的是( )
| A. | 核裂变是一种化学变化 | |
| B. | 12753I的质量数为127,原子序数为53,核内有74个中子 | |
| C. | 碘12753I和放射性碘13153I属于同素异形体 | |
| D. | 12753I与13153I是同一种核素 |
1.某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热△H为-55.2kJ/mol.(保留三位有效数字)
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.4 |
| 2 | 20.2 | 20.4 | 23.6 |
| 3 | 20.5 | 20.6 | 23.8 |
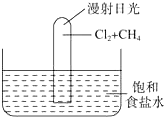 如图所示实验,试推测可能观察到的现象是:
如图所示实验,试推测可能观察到的现象是: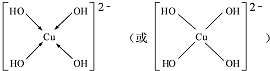 .(用→标出配位键)1mol[Cu (OH)4]2-中有8mol σ键.
.(用→标出配位键)1mol[Cu (OH)4]2-中有8mol σ键.