题目内容
14.科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4.
①Mn2+基态原子简化的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5)
②C、N、O第一电离能由大到小的顺序是:N>O>C
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O.
①Cu在周期表中ds区;
②CO的结构式:C≡O
③1mol CO2 中含有的π键数目为2×6.02×1023个(或2 mol)
(3)向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4]2-.不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
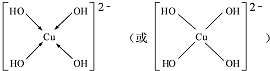 .(用→标出配位键)1mol[Cu (OH)4]2-中有8mol σ键.
.(用→标出配位键)1mol[Cu (OH)4]2-中有8mol σ键.
分析 (1)①Mn的原子序数为25,根据能量最低原理可写出Mn的基态原子的电子排布式,进而可确定Mn2+基态的电子排布式;
②同一周期元素,元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,据此判断第一电离能大小顺序;
(2)①周期表分为s区、p区、d区、ds区、f区,根据Cu的外围电子排布式分析;
②根据N2与CO为等电子体,结合等电子体结构相似判断;
③双键含有1个σ键和1个π键,CO2中含有2个双键;
(3)[Cu(OH)4]2-中与Cu2+与4个OH-形成配位键,配位键和O-H键都属于σ键.
解答 解:(1)①Mn的原子序数为25,基态原子的电子排布式为,1s22s22p63s23p63d54s2,则Mn2+基态的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5),
故答案为:1s22s22p63s23p63d5(或[Ar]3d5);
②同一周期元素,元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,C、N、O元素处于同一周期且原子序数逐渐增大,N处于第VA族,所以第一电离能N>O>C,
故答案为:N>O>C;
(2)①Cu元素原子核外电子数为29,其基态原子的电子排布式为1s22s22p63s23p63d104s1,周期表分为s区、p区、d区、ds区、f区,Cu的外围电子排布式为3d104s1,Cu属于第IB族元素,在周期表中位于ds区,
故答案为:ds;
②N2与CO为等电子体,二者结构相似,N2的结构为N≡N,则CO的结构为C≡O,
故答案为:C≡O;
③双键含有1个σ键和1个π键,CO2结构式为O=C=O,含有2个双键,则1mol CO2 中含有的π键数目为2×6.02×1023个(或2 mol),
故答案为:2×6.02×1023个(或2 mol);
(3)[Cu(OH)4]2-中与Cu2+与4个OH-形成配位键,则[Cu(OH)4]2-的结构可用示意图表示为: ,配位键和O-H键都属于σ键,所以1mol[Cu (OH)4]2-中有8molσ键,
,配位键和O-H键都属于σ键,所以1mol[Cu (OH)4]2-中有8molσ键,
故答案为 ;8.
;8.
点评 本题综合考查物质的结构与性质知识,侧重于电子排布式、第一电离能、配位键等知识,题目难度中等,注意把握配位键的判断方法,试题知识点较多、综合性较强,充分考查了学生的灵活应用能力.

 名校课堂系列答案
名校课堂系列答案| A. | Na2CO3和H2SO4 | B. | Na2SO3和盐酸 | C. | Na2S和HCl | D. | Na2SO3和H2SO4 |
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A. | 反应开始20 s内以二氧化氮表示的平均反应速率为0.00125 mol/L•s | |
| B. | 80 s时向容器中加入0.32 mol氦气,同时将容器扩大为 4 L,则平衡将不移动 | |
| C. | 当反应达到平衡后,若缩小容器的体积,平衡向生成N2O4方向移动,气体的颜色变深 | |
| D. | 若其它条件不变,起始投料改为0.40 mol N2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等 |
| A. | 核内有2个质子 | B. | 与4He互为同位素 | ||
| C. | 核内有1个中子 | D. | 是4He的同素异形体 |
| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 将A、B组成原电池时,A为正极 | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 将A和B用导线相连接,一同放入CuSO4溶液中,B的表面有红色的铜析出 |
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化.反应的化学方程式为2NO(g)+2CO( g)?N2( g)+2CO2(g).
①已知部分化学键的键能如下:
| 分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O=C=O | N2/N≡N |
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
②若上述反应在恒温、恒容的密闭体系中进行,并在t.时刻达到平衡状态,则下列示意图不符合题意的是ABC(填选项字母).(下图中V正、K、n、P总分别表示正反应速率、平衡常数、物质的量和总压强)
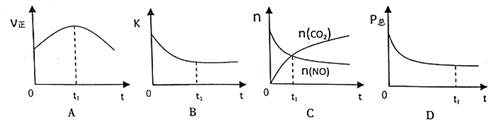
③在T℃下,向体积为10L的恒容密闭容器中通人NO和CO,测得了不同时间时NO和CO的物质的量如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/×10-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n(CO)/×10-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
(2)是硫酸工业释放出的主要尾气,为减少对环境造成的影响,采用以下方法将其资源化利用,重新获得重要工业产品硫化钙.
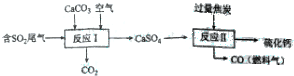
①写出反应的化学方程式2CaCO3+O2+2SO2=2CaSO4+2CO2.
②反应中每生成1mol硫化钙理论上转移电子数为8NA.
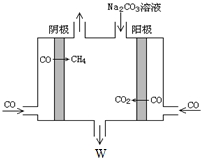
③为充分利用副产品CO,设计电解CO制备CH4和W,工作原理如图所示,生成物W是NaHCO3,其原理用电解总离子方程式解释是4CO+3CO32-+5H2O=6HCO3-+CH4↑.
| A. | 最高正化合价:③>②>① | B. | 单质氧化性:③>①>② | ||
| C. | 电负性:③>②>① | D. | 原子半径:③>②>① |