题目内容
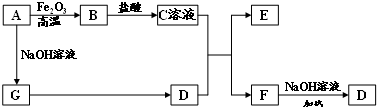
如图1表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去).其中A为单质;D有漂白性;在实验室中,常用固体B和固体C加热制取气体F; F与G的组成元素相同,G与H分子所含电子数相同.请回答:

(1)D的名称 ,B中化学键类型 .
(2)G的电子式为 ;反应④过程中能看到的现象 .
(3)写出反应②化学方程式:
(4)向D的溶液加入H的浓溶液有A生成,其反应的离子方程式为: .
(5)写出反应③的化学方程式 .
(6)将H和F分别装入如图2烧瓶中,通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是 .

(1)D的名称
(2)G的电子式为
(3)写出反应②化学方程式:
(4)向D的溶液加入H的浓溶液有A生成,其反应的离子方程式为:
(5)写出反应③的化学方程式
(6)将H和F分别装入如图2烧瓶中,通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是
考点:无机物的推断
专题:推断题
分析:在实验室中,常用固体B和固体C加热制取气体F,应为NH4Cl和Ca(OH)2反应生成氨气的反应,则F为NH3,E为CaCl2,根据F可与H生成C,则C为NH4Cl,B为Ca(OH)2,H为HCl,根据F与G的组成元素相同,G与I(为HCl,含有18个电子)分子所含电子数相同,则G为N2H4,D具有漂白性,可知D为Ca(ClO)2,则A为Cl2,以此来回答题中各问题.
解答:
解:在实验室中,常用固体B和固体C加热制取气体F,应为NH4Cl和Ca(OH)2反应生成氨气的反应,则F为NH3,E为CaCl2,根据F可与H生成C,则C为NH4Cl,B为Ca(OH)2,H为HCl,根据F与G的组成元素相同,G与I(为HCl,含有18个电子)分子所含电子数相同,则G为N2H4,D具有漂白性,可知D为Ca(ClO)2,则A为Cl2,
(1)由上述分析可知,D的名称为:次氯酸钙,B为Ca(OH)2,含有离子键、共价键,故答案为:次氯酸钙;离子键、共价键;
(2)G为N2H4,电子式为 ;反应④是氨气与HCl反应生成氯化铵,能看到的现象是:有白烟产生,
;反应④是氨气与HCl反应生成氯化铵,能看到的现象是:有白烟产生,
故答案为: ;有白烟产生;
;有白烟产生;
(3)反应②化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(4)向次氯酸钙的溶液加入HCl的浓溶液有氯气生成,其反应的离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
(5)根据反应物和生成物结合质量守恒定律,可知反应③的化学方程式为:Ca(ClO)2+4NH3═CaCl2+2N2H4+2H2O,故答案为:Ca(ClO)2+4NH3═CaCl2+2N2H4+2H2O;
(6)将HCl和氨气分别装入如图2烧瓶中,通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是:关闭b打开a、c,然后挤压胶头滴管,接下来关闭a打开b、c,即在I中形成喷泉,
故答案为:关闭b打开a、c,然后挤压胶头滴管,接下来关闭a打开b、c,即在I中形成喷泉.
(1)由上述分析可知,D的名称为:次氯酸钙,B为Ca(OH)2,含有离子键、共价键,故答案为:次氯酸钙;离子键、共价键;
(2)G为N2H4,电子式为
 ;反应④是氨气与HCl反应生成氯化铵,能看到的现象是:有白烟产生,
;反应④是氨气与HCl反应生成氯化铵,能看到的现象是:有白烟产生,故答案为:
 ;有白烟产生;
;有白烟产生;(3)反应②化学方程式为:2NH4Cl+Ca(OH)2
| ||
| ||
(4)向次氯酸钙的溶液加入HCl的浓溶液有氯气生成,其反应的离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
(5)根据反应物和生成物结合质量守恒定律,可知反应③的化学方程式为:Ca(ClO)2+4NH3═CaCl2+2N2H4+2H2O,故答案为:Ca(ClO)2+4NH3═CaCl2+2N2H4+2H2O;
(6)将HCl和氨气分别装入如图2烧瓶中,通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是:关闭b打开a、c,然后挤压胶头滴管,接下来关闭a打开b、c,即在I中形成喷泉,
故答案为:关闭b打开a、c,然后挤压胶头滴管,接下来关闭a打开b、c,即在I中形成喷泉.
点评:本题考查元素化合物的推断,题目较为综合,具有一定难度,充分利用题目给予的信息进行推断,进行猜测验证,掌握元素化合物性质是关键,注意元素化合物基础知识的积累.

练习册系列答案
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
为了增强漂白粉漂白能力,对漂白粉溶液作如下处理,其中达不到目的操作是( )
| A、加烧碱溶液 |
| B、加醋酸溶液 |
| C、通CO2气体 |
| D、微热 |

 向2L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示[t0~15s阶段n(B)未画出].图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段所改变的外界条件均不同.已知t3~t4阶段为使用催化剂.观察如图,回答以下问题:
向2L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示[t0~15s阶段n(B)未画出].图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段所改变的外界条件均不同.已知t3~t4阶段为使用催化剂.观察如图,回答以下问题: