题目内容
图2是研究甲烷取代反应实验装置图,具体的实验方法是:取一个100mL的大量筒,先后收集20mL CH4和80mL Cl2,进行实验.

(1)实验室制取氯气的装置如图1所示,请写出烧瓶中的反应方程式为: 浓盐酸在反应中体现了 性和 性.
(2)下列常用的干燥剂中,不能干燥氯气的是
A、浓硫酸 B、P2O5 C、无水氯化钙 D、碱石灰
(3)氯气是 色的有毒气体,实验中剩余的氯气可用NaOH溶液吸收,请写出发生的离子方程式: .
(4)若研究甲烷与氯气的取代反应,还需要的条件是 .若将如图2所示装置放在强光下照射会有 (填可能发生的不良后果).
(5)若量筒中的甲烷和氯气的量比较大,放在光亮的地方足够长的时间,下方水槽中的现象是 ,产生此现象的原因 (用文字和方程式说明)

(1)实验室制取氯气的装置如图1所示,请写出烧瓶中的反应方程式为:
(2)下列常用的干燥剂中,不能干燥氯气的是
A、浓硫酸 B、P2O5 C、无水氯化钙 D、碱石灰
(3)氯气是
(4)若研究甲烷与氯气的取代反应,还需要的条件是
(5)若量筒中的甲烷和氯气的量比较大,放在光亮的地方足够长的时间,下方水槽中的现象是
考点:甲烷的取代反应,甲烷的性质实验
专题:实验设计题
分析:(1)实验室用浓盐酸与二氧化锰加热制取氯气;浓盐酸在反应中既表现了还原性,又表现出酸性;
(2)氯气为酸性气体,不能使用碱性干燥剂干燥;
(3)氯气为黄绿色的有毒气体,制取氯气的尾气表现使用氢氧化钠溶液吸收,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(4)甲烷与氯气的反应需要在光照条件下进行,但是不是在强光下照射,否则容易发生爆炸;
(5)氯气与甲烷反应生成氯代甲烷及氯化氢,氯化氢溶于水电离出氯离子,所以水槽中有氯化银沉淀生成.
(2)氯气为酸性气体,不能使用碱性干燥剂干燥;
(3)氯气为黄绿色的有毒气体,制取氯气的尾气表现使用氢氧化钠溶液吸收,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(4)甲烷与氯气的反应需要在光照条件下进行,但是不是在强光下照射,否则容易发生爆炸;
(5)氯气与甲烷反应生成氯代甲烷及氯化氢,氯化氢溶于水电离出氯离子,所以水槽中有氯化银沉淀生成.
解答:
解:(1)实验室制取氯气用二氧化锰氧化浓盐酸,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,在反应中还生成氯化锰和水,所以盐酸的作用除起酸性的作用外,还起酸性的作用,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;还原;酸;
(2)氯气是一种酸性气体,不能用碱性干燥剂进行干燥,因此不能选用D.碱石灰干燥,
故答案为:D;
(3)氯气是一种黄绿色有毒的气体,尾气处理时需要用氢氧化钠溶液吸收,反应的方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:黄绿;Cl2+2OH-═Cl-+ClO-+H2O;
(4)甲烷和氯气发生取代反应,还需要光照,但如果在强光下直接照射,则容易发生爆炸现象,
故答案为:光照;爆炸;
(5)甲烷和氯气发生取代反应,在生成卤代烃的同时,生成物中有氯化氢,氯化氢极易溶于水,和硝酸银反应生成氯化银,因此在水槽中会出现白色沉淀,
故答案为:出现白色沉淀;甲烷和氯气取代反应HCl溶于水,与硝酸银溶液作用产生难溶氯化银,Cl-+Ag+=AgCl↓.
| ||
故答案为:MnO2+4HCl(浓)
| ||
(2)氯气是一种酸性气体,不能用碱性干燥剂进行干燥,因此不能选用D.碱石灰干燥,
故答案为:D;
(3)氯气是一种黄绿色有毒的气体,尾气处理时需要用氢氧化钠溶液吸收,反应的方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:黄绿;Cl2+2OH-═Cl-+ClO-+H2O;
(4)甲烷和氯气发生取代反应,还需要光照,但如果在强光下直接照射,则容易发生爆炸现象,
故答案为:光照;爆炸;
(5)甲烷和氯气发生取代反应,在生成卤代烃的同时,生成物中有氯化氢,氯化氢极易溶于水,和硝酸银反应生成氯化银,因此在水槽中会出现白色沉淀,
故答案为:出现白色沉淀;甲烷和氯气取代反应HCl溶于水,与硝酸银溶液作用产生难溶氯化银,Cl-+Ag+=AgCl↓.
点评:本题考查氯气的实验室制法、甲烷的取代反应,题目难度中等,注意掌握实验室制取氯气的反应原理,明确甲烷的取代反应原理、反应条件,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
某混合溶液中含有HCO3-、CO32-、SO32-、SO42-、NO3-、K+、NH4+等七种离子,将过量的Na2O2固体加入其中后,这七种离子仍能大量存在的有( )
| A、2 种 |
| B、3 种 |
| C、4 种 |
| D、5 种 |
下列各种表述与示意图一致的是( )


| A、图①表示25℃用盐酸标准液滴定NaOH溶液时,溶液的pH值随盐酸体积的变化 |
| B、图②表示2SO2(g)+O2(g)?2SO3(g)△H<0正逆反应的平衡常数K随温度的变化 |
| C、图③表示往HCl、AlCl3、MgCl2混合液中滴加强碱溶液,沉淀质量随碱液体积的变化 |
| D、图④表示酸雨的pH值随放置时间的变化(不考虑水的自然挥发及温度变化) |
下列有关实验操作错误的是( )
| A、用药匙取用粉末状或小颗粒状固体 | ||
| B、称量固体NaOH的质量时,分别在两个托盘上垫上质量相同的滤纸 | ||
C、给盛有约
| ||
| D、加热蒸发皿时无需垫石棉网 |
下列装置中能构成原电池的是( )
A、 稀硫酸 稀硫酸 |
B、 稀硫酸 稀硫酸 |
C、 稀硫酸 稀硫酸 |
D、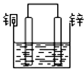 酒精 酒精 |

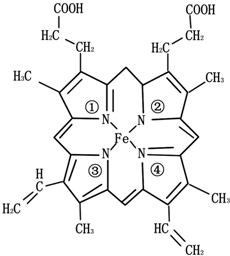 金属及其化合物在生产、生活中有广泛应用.
金属及其化合物在生产、生活中有广泛应用.