题目内容
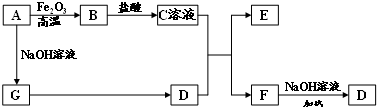
已知A~G有如图所示的转化关系(部分生成物已略去),其中A、G为单质,D是能使湿润的红色石蕊试纸变蓝色的气体,E、F均能与NaOH溶液反应.
请回答下列问题:
(1)写出F的电子式:
(2)①C溶液与D反应的离子方程式为
②F溶液与NaOH溶液共热反应的化学方程式为
(3)①请用离子方程式解释C溶液为何显酸性
②F溶液中离子浓度由大到小的顺序为
(4)将5.4gA投入200mL 2.0mol/L某溶液中有G单质产生,且充分反应后有金属剩余,则该溶液可能是 (填代号)
A.HNO3溶液 B.H2SO4溶液 C.NaOH溶液 D.HCl溶液
(5)将1molN2和3molG及催化剂充入容积为2L的某密闭容器中进行反应,已知该反应为放热反应.平衡时,测得D的物质的量浓度为a mol/L.
①如果反应速率v(G)=1.2mol/(L?min),则v(D)= mol/(L?min)
②在其他条件不变的情况下,若起始时充入0.5molN2和1.5molG达到平衡后,D的物质的量浓度 (填“大于”、“小于”或“等于”)a/2mol/L.
③该条件下的平衡常数为 (用含a的代数式表示)

请回答下列问题:
(1)写出F的电子式:
(2)①C溶液与D反应的离子方程式为
②F溶液与NaOH溶液共热反应的化学方程式为
(3)①请用离子方程式解释C溶液为何显酸性
②F溶液中离子浓度由大到小的顺序为
(4)将5.4gA投入200mL 2.0mol/L某溶液中有G单质产生,且充分反应后有金属剩余,则该溶液可能是
A.HNO3溶液 B.H2SO4溶液 C.NaOH溶液 D.HCl溶液
(5)将1molN2和3molG及催化剂充入容积为2L的某密闭容器中进行反应,已知该反应为放热反应.平衡时,测得D的物质的量浓度为a mol/L.
①如果反应速率v(G)=1.2mol/(L?min),则v(D)=
②在其他条件不变的情况下,若起始时充入0.5molN2和1.5molG达到平衡后,D的物质的量浓度
③该条件下的平衡常数为
考点:无机物的推断
专题:推断题
分析:D是能使湿润的红色石蕊试纸变蓝色的气体,则D为NH3,其中A、G为单质,且A与氧化铁反应,与氢氧化钠反应反应得到G,G反应可以得到氨气,可推知A为Al、G为H2,E、F均能与NaOH溶液反应,结合转化关系可知,故B为Al2O3,C为AlCl3,E为Al(OH)3,F为NH4Cl,据此解答.
解答:
解:D是能使湿润的红色石蕊试纸变蓝色的气体,则D为NH3,其中A、G为单质,且A与氧化铁反应,与氢氧化钠反应反应得到G,G反应可以得到氨气,可推知A为Al、G为H2,E、F均能与NaOH溶液反应,结合转化关系可知,故B为Al2O3,C为AlCl3,E为Al(OH)3,F为NH4Cl,
(1)F为NH4Cl,电子式为: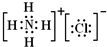 ,故答案为:
,故答案为: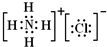 ;
;
(2)①C溶液与D反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
②F溶液与NaOH溶液共热反应的化学方程式为:NH4Cl+NaOH
NaCl+NH3↑+H2O,
故答案为:NH4Cl+NaOH
NaCl+NH3↑+H2O;
(3)①AlCl3溶液中铝离子水解:Al3++3H2O?Al(OH)3+3H+,平衡水的电离平衡,溶液呈酸性,
故答案为:Al3++3H2O?Al(OH)3+3H+;
②NH4Cl溶液中铵根离子水解,溶液呈酸性,故溶液中离子浓度由大到小的顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(4)将5.4g Al的物质的量=
=0.2mol,200mL 2.0mol/L某溶液中溶质的物质的量=0.2L×2mol/L=0.4mol,将Al投入该溶液中有G单质产生,且充分反应后有金属剩余,Al与稀硝酸反应没有气体单质生成,与稀硫酸、氢氧化钠、盐酸反应都生成氢气,
由2Al~3H2SO4可知,0.2molAl完全反应消耗H2SO4 的物质的量=0.3mol<0.4mol,故Al没有剩余,
由2Al~2NaOH可知,0.2molAl完全反应消耗NaOH的物质的量=0.2mol<0.4mol,故Al没有剩余,
由2Al~6HCl可知,0.2molAl完全反应消耗HCl的物质的量=0.6mol>0.4mol,故Al有剩余,
故答案为:D;
(5)将1molN2和3molH2和及催化剂充入容积为2L的某密闭容器中进行反应,已知该反应为放热反应.平衡时,测得NH3的物质的量浓度为a mol/L,
①如果反应速率v(H2)=1.2mol/(L?min),则v(NH3)=
v(H2)=
×1.2mol/(L?min)=0.8mol/(L?min),故答案为:0.8;
②在其他条件不变的情况下,若起始时充入0.5molN2和1.5molH2达到平衡等效为在原平衡基础上体积扩大一倍,压强减小,平衡向生成氮气、氢气的方向移动,故NH3的物质的量浓度小于0.5amol/L,故答案为:小于;
③N2(g)+3H2(g)?2NH3(g)
开始(mol/L):0.5 1.5 0
变化(mol/L):0.5a 1.5a a
平衡(mol/L):0.5(1-a) 1.5(1-a) a
故该温度下平衡常数k=
,
故答案为:
.
(1)F为NH4Cl,电子式为:
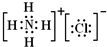 ,故答案为:
,故答案为: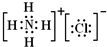 ;
;(2)①C溶液与D反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
②F溶液与NaOH溶液共热反应的化学方程式为:NH4Cl+NaOH
| ||
故答案为:NH4Cl+NaOH
| ||
(3)①AlCl3溶液中铝离子水解:Al3++3H2O?Al(OH)3+3H+,平衡水的电离平衡,溶液呈酸性,
故答案为:Al3++3H2O?Al(OH)3+3H+;
②NH4Cl溶液中铵根离子水解,溶液呈酸性,故溶液中离子浓度由大到小的顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(4)将5.4g Al的物质的量=
| 5.4g |
| 27g/mol |
由2Al~3H2SO4可知,0.2molAl完全反应消耗H2SO4 的物质的量=0.3mol<0.4mol,故Al没有剩余,
由2Al~2NaOH可知,0.2molAl完全反应消耗NaOH的物质的量=0.2mol<0.4mol,故Al没有剩余,
由2Al~6HCl可知,0.2molAl完全反应消耗HCl的物质的量=0.6mol>0.4mol,故Al有剩余,
故答案为:D;
(5)将1molN2和3molH2和及催化剂充入容积为2L的某密闭容器中进行反应,已知该反应为放热反应.平衡时,测得NH3的物质的量浓度为a mol/L,
①如果反应速率v(H2)=1.2mol/(L?min),则v(NH3)=
| 2 |
| 3 |
| 2 |
| 3 |
②在其他条件不变的情况下,若起始时充入0.5molN2和1.5molH2达到平衡等效为在原平衡基础上体积扩大一倍,压强减小,平衡向生成氮气、氢气的方向移动,故NH3的物质的量浓度小于0.5amol/L,故答案为:小于;
③N2(g)+3H2(g)?2NH3(g)
开始(mol/L):0.5 1.5 0
变化(mol/L):0.5a 1.5a a
平衡(mol/L):0.5(1-a) 1.5(1-a) a
故该温度下平衡常数k=
| a2 |
| (0.5-0.5a)×(1.5-1.5a)3 |
故答案为:
| a2 |
| (0.5-0.5a)×(1.5-1.5a)3 |
点评:本题考查无机物推断,D的性质是推断突破口,再结合转化关系中特殊反应推断,题目比较综合,涉及常用化学用语、盐类水解、化学反应速率及化学平衡等,难度中等,注意元素化合物知识的掌握.

练习册系列答案
相关题目
氯化铁溶液和氢氧化铁胶体的共同性质是( )
| A、加入氢氧化钠溶液都产生沉淀 |
| B、密封保存一段时间都产生沉淀 |
| C、分散质粒子都能透过半透膜 |
| D、前者电中性,后者带正电荷 |
下列有关实验操作错误的是( )
| A、用药匙取用粉末状或小颗粒状固体 | ||
| B、称量固体NaOH的质量时,分别在两个托盘上垫上质量相同的滤纸 | ||
C、给盛有约
| ||
| D、加热蒸发皿时无需垫石棉网 |
下列离子检验的方法正确的是( )
A、某溶液
| ||
B、某溶液
| ||
C、某溶液
| ||
D、某溶液
|
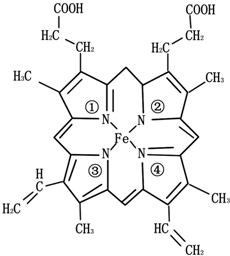 金属及其化合物在生产、生活中有广泛应用.
金属及其化合物在生产、生活中有广泛应用.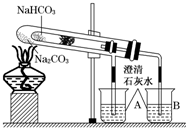 “套管实验”是将一支较小的试管装入另一试管中,经组装来完成原来需要两只或更多试管进行的实验.因其有许多优点,近年来被广泛开发并应用于化学实验中.下面这个实验为“套管实验”,实验装置中,小试管中部有沾上无水硫酸铜粉末的脱脂棉.请观察实验装置,分析实验原理,并回答下列问题:
“套管实验”是将一支较小的试管装入另一试管中,经组装来完成原来需要两只或更多试管进行的实验.因其有许多优点,近年来被广泛开发并应用于化学实验中.下面这个实验为“套管实验”,实验装置中,小试管中部有沾上无水硫酸铜粉末的脱脂棉.请观察实验装置,分析实验原理,并回答下列问题: