题目内容
铁、钴、镍的原子序数分别为26、27、28,它们的性质相似,被称为铁系元素.已知反应Fe2O3+6HCl=2FeCl3+3H2O,Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,则下列物质的氧化能力由强到弱的顺序是( )
| A、Fe2O3>Co2O3>Cl2 |
| B、Cl2>Fe2O3>Co2O3 |
| C、Cl2>Co2O3>Fe2O3 |
| D、Co2O3>Cl2>Fe2O3 |
考点:氧化性、还原性强弱的比较
专题:
分析:氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,根据方程式中元素的化合价变化判断氧化剂和氧化产物.
解答:
解:在Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O中,氧化剂是Co2O3,氧化产物是Cl2,所以氧化性Co2O3>Cl2;
Fe2O3+6HCl=2FeCl3+3H2O该反应是非氧化还原反应,说明Fe2O3不能氧化HCl,所以氧化性Cl2>Fe2O3;
故氧化性由强到弱的顺序是:Co2O3>Cl2>Fe2O3
故选D.
Fe2O3+6HCl=2FeCl3+3H2O该反应是非氧化还原反应,说明Fe2O3不能氧化HCl,所以氧化性Cl2>Fe2O3;
故氧化性由强到弱的顺序是:Co2O3>Cl2>Fe2O3
故选D.
点评:本题考查氧化性强弱的判断,难度不大.要注意在氧化还原反应中:氧化剂的氧化性强于氧化产物的氧化性.

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、某无色溶液中:Al3+、Cu2+、SO42-、Cl- |
| B、由水电离的c(H+)=1×10-12 mol?L-1的溶液中:Ba2+、K+、Cl-、NO3- |
| C、c(OH-)/c(H+)=1012的溶液中:Na+、Mg2+、NO3-、Cl- |
| D、加入足量过氧化钠后的溶液中:Mg2+、K+、Cl-、SO32- |
1mol碳完全燃烧后可放出393.5KJ的热量,下列热化学方程式正确的是( )
| A、C(s)+O2(g)=CO2(g)△H=+393.5 kJ/mol | ||
B、C(s)+
| ||
| C、C+O2=CO2△H=-393.5 kJ/mol | ||
| D、C(s)+O2(g)=CO2(g)△H=-393.5 kJ/mol |
下列有关化学用语使用正确的是( )
A、CO2的电子式: | ||
B、核内有8个中子的碳原子:
| ||
C、钾离子结构示意图: | ||
D、二氧化硫分子比例模型: |
等质量的下列有机物完全燃烧时,耗氧量最大的是( )
| A、甲烷 | B、乙烯 | C、乙烷 | D、苯 |
下列离子方程式中正确的是( )
| A、金属钠与水反应:Na+H2O═Na++OH-+H2↑ |
| B、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| C、实验室制备氢氧化铝:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| D、向稀盐酸溶液中加铁粉:3Fe+6H+=2Fe3++3H2↑ |
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.2 mol/L与0.1mol/L 醋酸溶液中c(H+)之比>2:1 |
| B、向0.1 mol/L 醋酸钠溶液中加入适量盐酸,得到的中性溶液:c(Na+)>c(CH3COO-)>c(Cl-)=c(CH3COOH) |
| C、pH=4的H2S溶液与pH=10 的NaOH溶液等体积混合:c(Na+)>2c(S2- )+c(HS-) |
| D、已知0.1 mol/L的二元酸H2A溶液pH=4.0,则在NaHA溶液中一定有:2c(OH-)+c(A2-)=c(H2A)+2c(H+) |
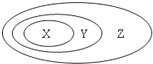 下表中所示物质或概念间的从属关系一定符合如图的是( )
下表中所示物质或概念间的从属关系一定符合如图的是( )