题目内容
19.某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去).其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO.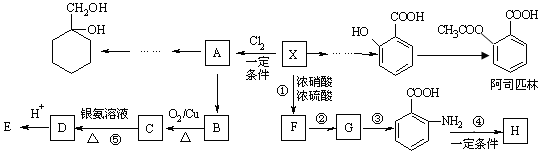
已知:

(1)F的结构简式是
 ,反应①~⑤中属于取代反应的有①.
,反应①~⑤中属于取代反应的有①.(2)反应②③两步能否互换不能(填“能”或“不能”),理由是防止氨基被氧化.
(3)B→C的化学方程式是
 .
.(4)
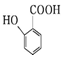 有多种同分异构体,请写出符合下列条件的同分异构体的结构简式
有多种同分异构体,请写出符合下列条件的同分异构体的结构简式 (或
(或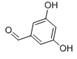 )(任写一种)
)(任写一种)①能发生银镜反应
②含有苯环且分子中有四种不同化学环境的氢原子
③1mol该有机物最多能与2molNaOH反应.
(5)请用合成反应流程图表示出由
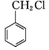 和其他无机试剂合成
和其他无机试剂合成 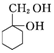 最合理的方案.
最合理的方案.示例:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
分析 相对分子质量为92的某芳香烃X,令其分子组成为CxHy,分子中最大碳原子数为$\frac{92}{12}$=7…8,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃X的分子式为C7H8,其结构简式为 ,X与氯气发生取代反应生成A为卤代烃,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,则A为
,X与氯气发生取代反应生成A为卤代烃,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,则A为 、B为
、B为 、C为
、C为 ,D酸化生成E,故D为
,D酸化生成E,故D为 ,E为
,E为 ;由甲苯与反应③的产物结构,结合苯胺容易被氧化,应先用酸性高锰酸钾氧化甲基为-COOH,再还原硝基为氨基,故
;由甲苯与反应③的产物结构,结合苯胺容易被氧化,应先用酸性高锰酸钾氧化甲基为-COOH,再还原硝基为氨基,故 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F为
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F为 ,F被酸性高锰酸钾氧化得到G为
,F被酸性高锰酸钾氧化得到G为 ,G在Fe/HCl条件下硝基被还原生成
,G在Fe/HCl条件下硝基被还原生成 ,H是一种功能高分子,链节组成为C7H5NO,与
,H是一种功能高分子,链节组成为C7H5NO,与 的分子式相比减少1分子H2O,该反应为
的分子式相比减少1分子H2O,该反应为 通过形成肽键发生缩聚反应生成高聚物,则H为
通过形成肽键发生缩聚反应生成高聚物,则H为 ;
;
(5)中 在催化剂条件下发生加成反应生成
在催化剂条件下发生加成反应生成 ,再在氢氧化钠醇溶液、加热条件下发生消去反应生成
,再在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,与氯气发生加成反应生成
,与氯气发生加成反应生成 ,最后在氢氧化钠水溶液中发生水解反应生成
,最后在氢氧化钠水溶液中发生水解反应生成 ,据此进行解答.
,据此进行解答.
解答 解:相对分子质量为92的某芳香烃X,令其分子组成为CxHy,分子中最大碳原子数为$\frac{92}{12}$=7…8,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃X的分子式为C7H8,其结构简式为 ;X与氯气发生取代反应生成A为卤代烃,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,则A为
;X与氯气发生取代反应生成A为卤代烃,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,则A为 ,B为
,B为 ,C为
,C为 ,D酸化生成E,故D为
,D酸化生成E,故D为 ,E为
,E为 .由甲苯与反应③的产物结构,结合苯胺容易被氧化,应先用酸性高锰酸钾氧化甲基为-COOH,再还原硝基为氨基,故
.由甲苯与反应③的产物结构,结合苯胺容易被氧化,应先用酸性高锰酸钾氧化甲基为-COOH,再还原硝基为氨基,故 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F为
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F为 ,F被酸性高锰酸钾氧化得到G为
,F被酸性高锰酸钾氧化得到G为 ,G再Fe/HCl条件下硝基被还原生成
,G再Fe/HCl条件下硝基被还原生成 ,H是一种功能高分子,链节组成为C7H5NO,与
,H是一种功能高分子,链节组成为C7H5NO,与 的分子式相比减少1分子H2O,该反应为
的分子式相比减少1分子H2O,该反应为 通过形成肽键发生缩聚反应生成高聚物,则H为
通过形成肽键发生缩聚反应生成高聚物,则H为 ,
,
(1)根据分析可知,F的结构简式为: ;
;
反应①是 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F ;
;
反应②是 在酸性高锰酸钾条件下反应氧化反应生成
在酸性高锰酸钾条件下反应氧化反应生成 ,该反应为氧化反应;
,该反应为氧化反应;
反应③为G在Fe/HCl条件下硝基被还原生成 ,该反应为还原反应;
,该反应为还原反应;
反应④为 通过形成肽键发生缩聚反应生成高聚物H
通过形成肽键发生缩聚反应生成高聚物H ,该反应为缩聚反应;
,该反应为缩聚反应;
反应⑤是C 与银氨溶液生成
与银氨溶液生成 :
: ,该反应为氧化反应,
,该反应为氧化反应,
根据分析可知,属于取代反应的为①,
故答案为: ;①;
;①;
(2)反应②是 在酸性高锰酸钾条件下反应氧化反应生成
在酸性高锰酸钾条件下反应氧化反应生成 ,反应③为G在Fe/HCl条件下硝基被还原生成
,反应③为G在Fe/HCl条件下硝基被还原生成 ,若反应②③两步不能互换,否则氨基会被氧化,
,若反应②③两步不能互换,否则氨基会被氧化,
故答案为:不能;防止氨基被氧化;
(3)B→C的化学方程式是: ,
,
故答案为: ;
;
(4) 的同分异构体中,①能发生银镜反应,说明分子中含有醛基;②含有苯环且分子中有四种不同化学环境的氢原子;③1mol该有机物最多能与2molNaOH反应,说明该有机物分子中1个酚羟基、1个羧基或含有2个酚羟基,满足体积的有机物如
的同分异构体中,①能发生银镜反应,说明分子中含有醛基;②含有苯环且分子中有四种不同化学环境的氢原子;③1mol该有机物最多能与2molNaOH反应,说明该有机物分子中1个酚羟基、1个羧基或含有2个酚羟基,满足体积的有机物如 或
或 ,
,
故答案为: (或
(或 );
);
(5) 在催化剂条件下发生加成反应生成
在催化剂条件下发生加成反应生成 ,再在氢氧化钠醇溶液、加热条件下发生消去反应生成
,再在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,与氯气发生加成反应生成
,与氯气发生加成反应生成 ,最后在氢氧化钠水溶液中发生水解反应生成
,最后在氢氧化钠水溶液中发生水解反应生成 ,合成反应流程图为:
,合成反应流程图为:
故答案为: .
.
点评 本题考查有机物的推断与合成,根据X的相对分子质量推断X的结构是解题的关键,结合B可以连续发生氧化反应及反应③的产物结构进行推断,是对有机物知识的综合考查,能较好的考查学生的自学能力、分析推理能力,是有机热点题型,难度中等.

| A. | 常温下,5.6g金属铁投入足量的浓硫酸中,电子转移数为0.3NA | |
| B. | 18g D2O所含的中子数为10NA | |
| C. | 标准状况下,8 gSO3所含原子数为0.4NA | |
| D. | 常温下,1.0LpH=13的Ba (OH) 2溶液中含有的OH-数目为0.2NA |
| A. | 氨水和盐酸 | B. | 氢氧化钠溶液和醋酸 | ||
| C. | 硫酸和氢氧化钡溶液 | D. | 硝酸和石灰水 |
| A. | 3种溶液中pH最小的是① | |
| B. | 3种溶液中水的电离程度最大的是② | |
| C. | ①与②等体积混合后溶液显酸性 | |
| D. | ①与③等体积混合后c(H+)>c(CH3COO-)>c(OH-) |
| A. | 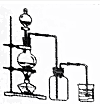 制备纯氯气 | B. | 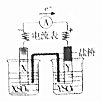 探究X、Y金属活泼性强弱 | ||
| C. |  证明H2CO3酸性比H2SiO3强 | D. |  制备无水氯化铁 |
 .
.