题目内容
15.下列有关物质的用途中,运用了物质的化学性质的是( )| A. | 用胶状氢氧化铝凝聚水中的悬浮物进行净水 | |
| B. | 用红棕色氧化铁制造红色油漆 | |
| C. | 氢氧化铝作为医用的胃酸中和剂 | |
| D. | 用氧化铝制造耐火坩埚和耐火管 |
分析 A.氢氧化铝胶体具有吸附性;
B.依据氧化铁为红棕色固体性质解答;
C.氢氧化铝碱性较弱,能够与盐酸反应;
D.耐火材料具有较高的熔点.
解答 解:A.氢氧化铝胶体具有吸附性,能够吸附水中固体杂质颗粒,用于净水为物理吸附过程,故A不选;
B.用红棕色氧化铁制造红色油漆,是利用氧化铁为红棕色物理性质解答,故B不选;
C.氢氧化铝碱性较弱,能够与盐酸反应,可以作为医用的胃酸中和剂,故C选;
D.耐火材料具有较高的熔点,氧化铝具有较高的熔点,氧化铝制造耐火坩埚和耐火管,利用氧化铝高熔点的物理性质,故D不选;
故选:C.
点评 本题考查了物质的性质与用途之间的关系,明确化学性质与物理性质差别,熟悉相关物质的性质是解题关键,题目难度不大,注意积累.

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
5.未来新能源的特点是资源丰富,在使用过程中对环境无污染或污染很小,且可以再生.下列属于未来新能源开发方向的是 ( )
①天然气 ②煤 ③燃料电池 ④太阳能 ⑤生物质能 ⑥风能 ⑦氢能.
①天然气 ②煤 ③燃料电池 ④太阳能 ⑤生物质能 ⑥风能 ⑦氢能.
| A. | ①②③④ | B. | ③④⑤⑥⑦ | C. | ②③⑤⑥⑦ | D. | ①④⑤⑥⑦ |
6.氯元素的相对原子质量为35.5,已知自然界中氯有35Cl、37Cl两种同位素原子,其中37Cl占质量分数为( )
| A. | 75% | B. | >75% | C. | <75% | D. | 不能确定 |
3.已知某溶液中含有Na+、Ca2+、Ag+三种阳离子,那么溶液中的阴离子可能是( )
| A. | NO3- | B. | Cl- | C. | Br- | D. | CO32- |
10.相同条件下,下列气体密度最大的是( )
| A. | 氯气 | B. | 二氧化硫 | C. | 氮气 | D. | 氢气 |
7.下列离子反应方程式正确的是( )
| A. | Cl2与水反应生成盐酸和次氯酸:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向氯化铝溶液中加入足量氨水:Al3++4NH3•H2O═AlO2-+2H2O+4NH4+ | |
| C. | 用醋酸除水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+H2O+CO2↑ | |
| D. | 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至呈中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ |
5.下列说法正确的是( )
| A. | 某盐溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+ | |
| B. | 某溶液中加入硝酸银溶液时,产生白色沉淀,说明原溶液中含有Cl- | |
| C. | 用铂丝蘸取某溶液在酒精灯上灼烧时,火焰呈黄色,说明原溶液中一定含有NaCl | |
| D. | 某溶液中加入BaCl2溶液生成白色沉淀,说明原溶液中有SO42- |
6.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | H2S的电子式 | B. | Cl-的结构示意图 | C. | CO2的电子式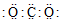 | D. | 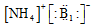 |