题目内容
15.下列离子方程式中正确的是( )| A. | 硫化钠水解:S2-+2H2O?H2S↑+2OH- | |
| B. | 硫氢化钠水解:HS-+H2O?H3O++S2- | |
| C. | 制Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| D. | 硫酸铝溶液跟偏铝酸钠溶液反应:Al3++3AlO2-+6H2O═4Al(OH)3↓ |
分析 A.多元弱酸根离子水解要分步进行,且不会生成硫化氢气体;
B.HS-水解生成硫化氢和氢氧根离子;
C.制备氢氧化铁胶体需要在加热条件下,且不能可逆号;
D.铝离子与偏铝酸根离子发生双水解反应生成氢氧化铝沉淀.
解答 解:A.多元弱酸根离子水解要分步进行,主要以第一步为主,则硫化钠正确的水解方程式为:S2-+H2O?HS-+OH-,故A错误;
B.HS-+H2O?H3O++S2-为电离方程式,硫氢化钠水解的离子方程式为:HS-+H2O?OH-+H2S,故B错误;
C.制Fe(OH)3胶体的离子方程式为:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故C错误;
D.硫酸铝溶液跟偏铝酸钠溶液反应生成氢氧化铝沉淀,反应的离子方程式为:Al3++3AlO2-+6H2O═4Al(OH)3↓,故D正确;
故选D.
点评 本题考查了离子方程式的书写,题目难度中等,涉及氢氧化铁胶体的制备、盐的水解原理及涉及离子方程式书写等知识,明确离子方程式的书写原则为解答关键,注意熟练掌握氢氧化铁胶体的制备方法.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
5.以 H、C、O、Na、Cl、Cu中一种或多种元素组成合适的物质,按下列要求完成各小题
(1)写出一种符合下列要求的物质的化学式:
(2)酸性氧化物和碱反应的化学方程式CO2+2NaOH=Na2CO3+2H2O
(3)难溶碱性氧化物和强酸反应的化学方程式CuO+2HCl═CuCl2+H2O.
(1)写出一种符合下列要求的物质的化学式:
| 分类标准 | 单质 | 碱性氧化物 | 酸性氧化物 | 含氧酸 | 盐 | 电解质 |
| 属于该类的物质 |
(3)难溶碱性氧化物和强酸反应的化学方程式CuO+2HCl═CuCl2+H2O.
6.下列物质能导电,且属于电解质的是( )
| A. | 铁丝 | B. | 盐酸 | C. | 酒精 | D. | 熔融的NaOH |
20.下列关于氯气的叙述正确的是( )
| A. | 氯气是无色、有刺激性气味的有毒气体 | |
| B. | 氯气在常压下冷却到-34.6℃变成液氯,它是易液化的气体之一 | |
| C. | 氢气在氯气中燃烧火焰呈淡蓝色 | |
| D. | 红热的铜丝放人氯气中生成绿色的氯化铜 |
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- | |
| C. | 无色透明的溶液中:MnO4-、SO42-、Na+、H+ | |
| D. | $\frac{KW}{c(H+)}$=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- |
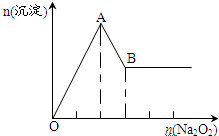 有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验
有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验