题目内容
9.过氧化尿素是一种新型漂白剂、消毒剂.合成过氧化尿素的流程及反应器的示意图如图: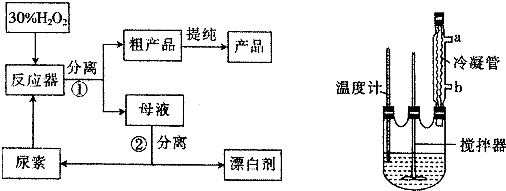
过氧化尿素的部分参数见表:
| 分子式 | 外观 | 热分解温度 | 熔点 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75~85℃ |
(2)反应器中发生反应的化学方程式为CO(NH2)2+H2O2=CO(NH2)2•H2O2;
(3)反应器中冷凝管中的冷水从b(填“a”或“b”)口流进,反应器加热温度不能太高的原因是温度过高,产品易分解,致使活性氧含量降低;
(4)搅拌器不能选择铁质或铝质材料的原因是铝、铁易被氧化;
(5)为测定产品中过氧化尿素的含量,称取干燥样品12.0g,溶于水,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL6mol/L硫酸,然后用0.20mol/L的KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如表:
| 实验序号 | 1 | 2 | 3 | |
| KMnO4溶液的体积/mL | 滴定前读数 | 0.00 | 0.00 | 2.00 |
| 滴定后读数 | 19.98 | 20.00 | 22.02 | |
②若滴定前滴定管尖嘴处无气泡,滴定后有气泡.则会使测得的过氧化尿素的含量偏低 (填“偏高”“偏低”或“不变”).
③产品中过氧化尿素的质最分数为78.3%.
分析 合成过氧化尿素是利用过氧化氢和尿素化合反应生成过氧化尿素,反应的化学方程式为:CO(NH2)2+H2O2=CO(NH2)2•H2O2,经过滤得到CO(NH2)2•H2O2粗产品,母液经分离得到尿素和漂白剂,漂白剂主要含有过氧化氢,
(1)过滤用到的玻璃仪器有漏斗、烧杯和玻璃棒;
(2)过氧化氢和尿素化合反应生成过氧化尿素;
(3)冷凝水应该从下口流入,温度过高,产品易分解;
(4)过氧化氢与Fe、Al反应.
(5)①酸性KMnO4溶液有强氧化性和酸性,应盛放在酸式滴定管中;
②依据滴定过程误差分析依据,c标准×V标准=c待测×V待测,产生误差的原因是标准液消耗的多少分析判断;
③已知尿素与KMnO4溶液不反应,发生的反应为5H2O2+2KMnO4+3H2SO4=8H2O+2MnSO4+K2SO4+5O2↑,根据高锰酸钾的物质的量求出H2O2和CO(NH2)2•H2O2的物质的量,再求出质量和质量分数.
解答 解:(1)流程中操作①是过滤,用到的玻璃仪器有漏斗、烧杯和玻璃棒,
故答案为:烧杯;玻璃棒;
(2)过氧化氢和尿素化合反应生成过氧化尿素,反应的化学方程式为:CO(NH2)2+H2O2=CO(NH2)2•H2O2,
故答案为:CO(NH2)2+H2O2=CO(NH2)2•H2O2;
(3)冷凝水应该从下口流入,这样冷凝效果好,故冷凝水从b口流入;CO(NH2)2•H2O2在45℃时发生分解,所以不能用酒精灯直接加热,应该用水浴加热;温度过高,产品易分解,致使活性氧含量降低,
故答案为:b;温度过高,产品易分解,致使活性氧含量降低;
(4)过氧化氢与Fe、Al反应生成三价铁离子,三价铁离子会加速过氧化氢的分解,所以搅拌器不能用铁质、铝质材料的,
故答案为:铝、铁易被氧化.
(5)①KMnO4溶液具有强氧化性,能将碱式滴定管下端的橡胶管氧化,所以不能用碱式滴定管量取,可以用酸式滴定管量取,滴定终点的现象为:滴入最后一滴KMnO4溶液时,溶液显浅红色,且半分钟内不褪色;
故答案为:酸;滴入最后一滴KMnO4溶液时,溶液显浅红色,且半分钟内不褪色;
②若滴定前滴定管尖嘴处无气泡,滴定后有气泡,依据反应的电离关系可知,5×c标准×V标准=c待测×V待测×2,测得标准液体积偏小,结果偏低,
故答案为:偏低;
③已知尿素与KMnO4溶液不反应,发生的反应为5H2O2+2KMnO4+3H2SO4=8H2O+2MnSO4+K2SO4+5O2↑,三次平均用去的KMnO4溶液为20.00mL
5H2O2~~~~~2KMnO4
5 2
nmol 0.2000mol•L-1×0.020L
则n=0.01mol,所以CO(NH2)2•H2O2为0.01mol,其质量为0.01mol×94g/mol=0.94g
所以产品中CO(NH2)2•H2O2的质量分数为$\frac{0.94g}{12g×\frac{25mL}{250mL}}$×100%=78.3%;
故答案为:78.3%.
点评 本题考查了物质制备实验过程分析判断,装置图的理解应用,为高频考点,把握发生的化学反应及实验操作为解答的关键,侧重分析能力及实验能力的考查,注意信息与所学知识的结合,题目难度较大.

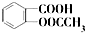 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

制备基本操作流程如下:
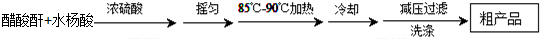
主要试剂和产品的物理常数如下表所示:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是醋酸酐和水易发生反应.
(2)合成阿司匹林时,最合适的加热方法是水浴加热.
(3)提纯粗产品流程如下,加热回流装置如图:
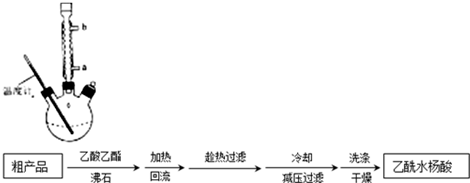
①使用温度计的目的是控制加热的温度,防止乙酰水杨酸受热易分解.
②冷凝水的流进方向是a(填“a”或“b”);
③趁热过滤的原因是防止乙酰水杨酸结晶析出.
④下列说法正确的是abc(填选项字母).
a.此种提纯方法中乙酸乙酯的作用是做溶剂
b.此种提纯粗产品的方法叫重结晶
c.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
d.可以用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为84.3%(用百分数表示,小数点后一位).
 水杨酸甲酯,是一种重要的有机合成原料.某化学小组用水杨酸(结构简式为
水杨酸甲酯,是一种重要的有机合成原料.某化学小组用水杨酸(结构简式为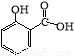 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.实验步骤:
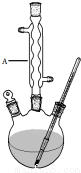
Ⅰ.如图,在三颈烧瓶中加入13.8g (0.1mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯9.12g.
常用物理常数:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是球形冷凝管.
(2)实验中加入甲苯对合成水杨酸甲酯的作用是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率.
(3)实验中加入无水硫酸镁的作用是干燥剂.
(4)反应结束后,分离出甲醇采用的方法是蒸馏(填操作名称).
(5)本实验的产率为60%.
| 熔点/℃ | 沸点/℃ | |
| 1-丁醇 | -89.53 | 117.25 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
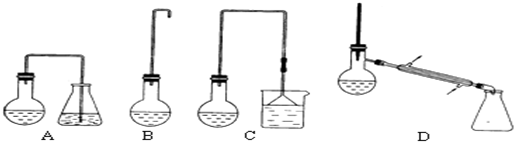
(1)制备1-溴丁烷的装置应选用上图中的C(填序号).反应加热时的温度不宜超过100℃,理由是防止1-溴丁烷因气化而逸出,影响产率且温度太高,浓硫酸氧化性增强,可能氧化溴化氢.
(2)制备操作中,加入的浓硫酸和溴化钠的作用是二者反应生成HBr.
(3)反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是D,(填序号);该操作应控制的温度(t)范围是101.6℃≤t<117.25℃.
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是c.(填字母)
a.NaI b.NaOH c.Na2SO3 d.KCl.
(1)实验室制备FeCO3的流程如下:
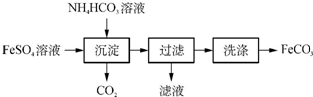
①写出生成沉淀的化学方程式:FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O.
②检验滤液中含有NH4+的方法是取少量滤液于试管中,加入足量NaOH溶液,加热,若产生气体可使湿润的红色石蕊试纸变蓝,则滤液中含有NH4+.
(2)甲同学为了验证FeCO3高温下煅烧是否得到Fe2O3,做了如表实验:
| 实验步骤 | 实验操作步骤 |
| Ⅰ | 取一定质量的FeCO3固体置于坩埚中,高温煅烧至质量不再减轻,冷却至室温 |
| Ⅱ | 取少量实验步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解 |
| Ⅲ | 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红 |
①实验步骤Ⅲ中溶液变红的离子方程式为Fe3++3SCN-=Fe(SCN)3.
②乙同学提出了不同的看法:煅烧产物可能是Fe3O4,因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+.于是乙同学对实验步骤Ⅲ进行了补充:另取少量实验步骤Ⅱ所得溶液,然后D(填字母),用来检验溶液中是否含有Fe2+.
A.滴加氯水B.滴加KSCN溶液
C.先滴加KSCN溶液后滴加氯水D.滴加酸性KMnO4溶液
(3)丙同学认为即使得到乙同学预期的实验现象,也不能确定煅烧产物即为Fe3O4.
①丙同学持此看法的理由是氧化亚铁、四氧化三铁中也是含有+2价铁元素的.
②丙同学查阅资料得知煅烧FeCO3的产物中含有+2价铁元素,于是他设计了由FeCO3制备Fe2O3的方案.先向FeCO3粉末中依次加入试剂:稀硫酸、氯水和氢氧化钠;然后再过滤(填操作)、洗涤、灼烧即可得到Fe2O3.
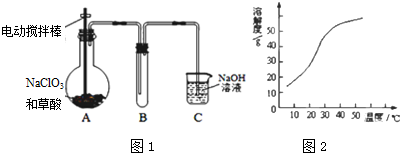
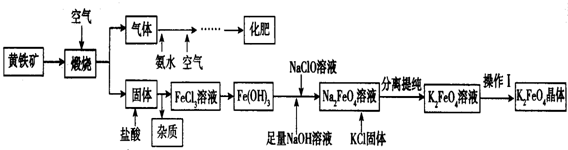
 甲组同学拟用高锰酸钾制取氧气,并收集和测量氧气体积,其装置如图所示.
甲组同学拟用高锰酸钾制取氧气,并收集和测量氧气体积,其装置如图所示.