题目内容
10.某原子的原子结构示意图为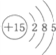 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该原子位于第三周期,ⅤA族 | B. | 该原子位于第五周期,ⅢB族 | ||
| C. | 该原子位于第三周期,ⅤB族 | D. | 该原子位于第五周期,ⅢA族 |
分析 主族元素周期数=电子层数、主族族序数=最外层电子数,据此判断.
解答 解: 由3个电子层,处于第三周期,最外层电子数为5,处于ⅤA族,故该元素处于第三周期第ⅤA族,故选A.
由3个电子层,处于第三周期,最外层电子数为5,处于ⅤA族,故该元素处于第三周期第ⅤA族,故选A.
点评 本题考查结构位置关系,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4. 向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
 向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液中:Na+、Mg2+、SO42-、HCO3- | |
| B. | b点对应的溶液中:Ag+、Ca2+、NO3-、F- | |
| C. | c点对应的溶液中:Na+、S2-、SO42-、Cl- | |
| D. | d点对应的溶液中:K+、NH4+、I-、CO32- |
2.在钢铁表面进行烤蓝(蓝色物质为Fe3O4,也可表示为FeFe2O4)的原理如下:
①3Fe+NaNO2+5NaOH═3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O═Fe3O4+4NaOH
下列说法中不正确的是( )
①3Fe+NaNO2+5NaOH═3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O═Fe3O4+4NaOH
下列说法中不正确的是( )
| A. | 反应②配平后,H2O的化学计量数为5 | |
| B. | Fe3O4既可看作是氧化物,又可看作是亚铁盐 | |
| C. | 反应③中,Na2Fe2O4是氧化剂,Na2FeO2是还原剂 | |
| D. | 碱性条件下,NaNO2的氧化性比Na2FeO2强 |
19.下列离子方程式表达正确的是( )
| A. | Ca(HCO3)2溶液与足量盐酸混合:Ca(HCO3)2+2H+═Ca2++2CO2↑+2H2O | |
| B. | Na2CO3溶液中通入CO2气体:CO${\;}_{3}^{2-}$+CO2+H2O═2HCO${\;}_{3}^{-}$ | |
| C. | 实验室用NH4Cl固体与Ca(OH)2固体混合制NH3:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO${\;}_{3}^{2-}$+2HClO |
20.用乙醇为原料制取乙二醇,可行的反应途径是( )
| A. | 氧化反应→加成反应→水解反应 | B. | 取代反应→水解反应→加成反应 | ||
| C. | 消去反应→酯化反应→水解反应 | D. | 消去反应→加成反应→水解反应 |

 2,4-二甲基已烷
2,4-二甲基已烷 3-甲基-1-丁烯
3-甲基-1-丁烯



 +3HO-NO2
+3HO-NO2
 +3H2O
+3H2O CH2=CHCl.
CH2=CHCl.