题目内容
5.某烃2.8g,在氧气中燃烧生成4.48L(标准状况)二氧化碳,3.6g水,它的相对分子质量是氢气的14倍,求此烃的化学式C2H4,写出它的结构简式CH2=CH2.分析 计算烃的相对分子质量,根据原子守恒确定烃的最简式,进而计算烃的分子式,书写其可能的结构简式.
解答 解:烃燃烧是二氧化碳为$\frac{4.48L}{22.4L/mol}$=0.2mol,水为$\frac{3.6g}{18g/mol}$=0.2mol,
它的相对分子质量是氢气的14倍,则相对分子质量为28,
2.8g烃的物质的量为$\frac{2.8g}{28g/mol}$=0.1mol,
可知1mol烃含有2molC,4molH,分子式为C2H4,结构简式为CH2=CH2,
故答案为:C2H4;CH2=CH2.
点评 本题考查有机物分子式确定,比较基础,注意理解掌握燃烧法利用原子守恒确定有机物分子式.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列表示物质结构的化学用语或模型图正确的是( )
| A. | H2O的结构式:H-O-H | B. | 乙烯的结构简式为CH2CH2 | ||
| C. | CO2的比例模型: | D. | 丙烯的电子式: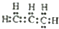 |
10.某原子的原子结构示意图为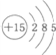 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该原子位于第三周期,ⅤA族 | B. | 该原子位于第五周期,ⅢB族 | ||
| C. | 该原子位于第三周期,ⅤB族 | D. | 该原子位于第五周期,ⅢA族 |
 .
.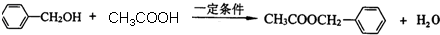 .
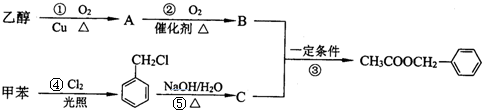
.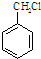 为原料经过三步反应合成
为原料经过三步反应合成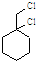 ,无机原料任选,写出反应的化学方程式:
,无机原料任选,写出反应的化学方程式: +H2$→_{△}^{催化剂}$
+H2$→_{△}^{催化剂}$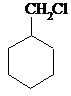
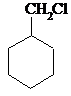 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$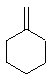 +NaCl+H2O
+NaCl+H2O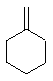 +Cl2→
+Cl2→ .
. .
.