题目内容
下列叙述不正确的是( )
| A、在标准状况下,将22.4L氨气溶于1L水中,得到1mol?L-1的氨水 |
| B、配制0.1mol?L-1的Na2CO3溶液480mL,需用500mL容量瓶 |
| C、10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49% |
| D、向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2、和Na2O,使溶液均恰好饱和则加入的Na2O2与Na2O的物质的量之比等于1:1(温度不变) |
考点:物质的量浓度的相关计算,溶液中溶质的质量分数及相关计算
专题:
分析:A.标准状况下22.4L氨气的物质的量为1mol,溶于1L水中,所带溶液体积不是1L,溶液浓度不是1mol/L;
B.实验室中没有480mL的容量瓶,配制480mL溶液,需要选用500mL的容量瓶;
C.10mL水的质量小于10mL硫酸溶液的质量,则混合液的质量小于原先硫酸溶液的质量的2倍;
D.等物质的量的过氧化钠、氧化钠与水反应生成氢氧化钠的物质的量相等.
B.实验室中没有480mL的容量瓶,配制480mL溶液,需要选用500mL的容量瓶;
C.10mL水的质量小于10mL硫酸溶液的质量,则混合液的质量小于原先硫酸溶液的质量的2倍;
D.等物质的量的过氧化钠、氧化钠与水反应生成氢氧化钠的物质的量相等.
解答:
解:A.标准状况下22.4L氨气的物质的量为1mol,将1mol氨气溶于1L水中,所带溶液的体积不是1L,得到溶液浓度不是1mol?L-1,故A错误;
B.配制0.1mol?L-1的Na2CO3溶液480mL,应该选用规格稍大于该体积且规格比较接近的容量瓶,所以配制时需要需用500mL容量瓶,故B正确;
C.硫酸的密度大于水,10mL质量分数为98%的H2SO4的质量大于10mL水,混合液质量小于原硫酸溶液质量的2倍,则混合液中H2SO4的质量分数大于49%,故C正确;
D.向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,由于等物质的量的过氧化钠、氧化钠与水反应生成的氢氧化钠的量相等,所以使溶液均恰好饱和时加入的Na2O2与Na2O的物质的量之比等于1:1(温度不变),故D正确;
故选A.
B.配制0.1mol?L-1的Na2CO3溶液480mL,应该选用规格稍大于该体积且规格比较接近的容量瓶,所以配制时需要需用500mL容量瓶,故B正确;
C.硫酸的密度大于水,10mL质量分数为98%的H2SO4的质量大于10mL水,混合液质量小于原硫酸溶液质量的2倍,则混合液中H2SO4的质量分数大于49%,故C正确;
D.向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,由于等物质的量的过氧化钠、氧化钠与水反应生成的氢氧化钠的量相等,所以使溶液均恰好饱和时加入的Na2O2与Na2O的物质的量之比等于1:1(温度不变),故D正确;
故选A.
点评:本题考查了物质的量浓度的计算、配制一定浓度的溶液方法、过氧化钠与氧化钠的性质,题目难度中等,试题知识点较多,充分考查了学生的分析、理解能力及对基础知识的把握情况,注意熟练掌握物质的量浓度的概念及计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述中,正确的是 ( )
| A、太阳能、核能和天然气都属于新型能源 |
| B、哥本哈根气候大会讨论的减排目标主要是控制二氧化硫排放 |
| C、84消毒液具有强氧化性,可杀死流感病毒 |
| D、比黄金还贵的18O2和普通的16O2是两种不同的核素 |
相同分子数的SO2和CO2中,相等的是( )
| A、原子总数 |
| B、电子个数 |
| C、物质质量 |
| D、氧元素的质量分数 |
下列各项内容中,排列顺序正确的是( )
| A、固体的热稳定性:Na2CO3>CaCO3>NaHCO3 |
| B、金属活动性Li>Na>K |
| C、氧化物的稳定性:H2Se>H2S |
| D、微粒半径:K+>S2->F- |
下列说法正确的是( )
| A、16O2与18O2互为同位素,H2O、D2O、T2O互为同素异形体,N60和N2互为同系物 |
| B、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| C、非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
D、Ca的原子结构示意图为 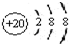 |
下列变化过程中,不涉及化学变化的是( )
| A、氯化钠的熔化 |
| B、碳的燃烧 |
| C、氨气溶于水 |
| D、水的通电分解 |
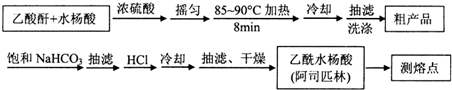
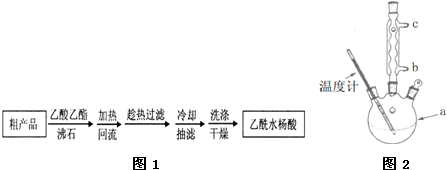
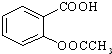 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水 S杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水 S杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: