题目内容
下列离子方程式书写正确的是( )
| A、CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓ |
| B、澄清石灰水与稀盐酸反应:OH-+H+=H2O |
| C、NaHSO3溶液与NaHSO4溶液混合:SO32-+2H+=H2O+SO2↑ |
| D、铁钉放入硫酸铜溶液中:Fe+3Cu2+=2Fe3++3Cu |
考点:离子方程式的书写
专题:
分析:A.漏写生成氢氧化铜的离子反应;
B.反应生成氯化钙和水;
C.亚硫酸氢根离子不能拆分;
D.反应生成硫酸亚铁和Cu.
B.反应生成氯化钙和水;
C.亚硫酸氢根离子不能拆分;
D.反应生成硫酸亚铁和Cu.
解答:
解:A.CuSO4溶液与Ba(OH)2溶液混合的离子反应为Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓,故A错误;
B.澄清石灰水与稀盐酸反应的离子反应为OH-+H+=H2O,故B正确;
C.NaHSO3溶液与NaHSO4溶液混合的离子反应为HSO3-+H+=H2O+SO2↑,故C错误;
D.铁钉放入硫酸铜溶液中的离子反应为Fe+Cu2+=Fe2++Cu,故D错误;
故选B.
B.澄清石灰水与稀盐酸反应的离子反应为OH-+H+=H2O,故B正确;
C.NaHSO3溶液与NaHSO4溶液混合的离子反应为HSO3-+H+=H2O+SO2↑,故C错误;
D.铁钉放入硫酸铜溶液中的离子反应为Fe+Cu2+=Fe2++Cu,故D错误;
故选B.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应及分析应用能力的考查,注意硫酸氢钠相当于一元强酸,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组混合物中,能用分液漏斗进行分离的是( )
| A、色拉油和水 |
| B、溴和四氯化碳 |
| C、乙醇和水 |
| D、汽油和煤油 |
在密闭容器中,反应2X(g)+Y2(g)?2XY(g);△H<0,达到甲平衡.在仅改变某一条件后,达到乙平衡,下列分析正确的是( )
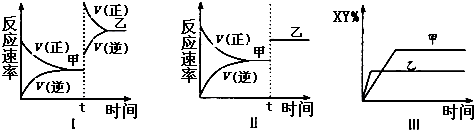

| A、图I中,甲、乙的平衡常数分别为K1、K2,则K1<K2 |
| B、图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低 |
| C、图Ⅱ中,t时间是增大了压强 |
| D、图Ⅲ是反应分别在甲、乙条件下达到平衡,说明乙温度高于甲 |
下列说法正确的是( )
| A、固体氯化钠不导电,所以氯化钠是非电解质 |
| B、铜丝能导电,所以铜是电解质 |
| C、氯化氢是电解质,其水溶液能导电 |
| D、CO2的水溶液能导电,所以CO2是电解质 |
下列物质的水溶液能够导电,但属于非电解质的是( )
| A、H2S |
| B、碳酸氢钠 |
| C、氨气 |
| D、氢氧化钾 |
在以离子键为主的化学键中常含有共价键的成分,下列各对原子形成化学键中共价键成分最少的是( )
| A、Cl,F | B、Na,F |
| C、Na,Cl | D、Mg,O |
在下列化学方程式中,能够用离子方程式H++OH-=H2O表示的是( )
| A、醋酸溶液与氢氧化钠溶液反应 |
| B、盐酸与氨水反应 |
| C、硫酸氢钠溶液与氢氧化钾溶液反应 |
| D、氢氧化铁与硫酸溶液反应 |