题目内容
在下列化学方程式中,能够用离子方程式H++OH-=H2O表示的是( )
| A、醋酸溶液与氢氧化钠溶液反应 |
| B、盐酸与氨水反应 |
| C、硫酸氢钠溶液与氢氧化钾溶液反应 |
| D、氢氧化铁与硫酸溶液反应 |
考点:离子方程式的书写
专题:
分析:能用离子方程式H++OH-=H2O表示的化学反应应为强酸和可溶性强碱之间的反应生成可溶性盐和水的反应,弱酸和弱碱应写成化学式,离子方程式中不能拆开,如:醋酸、一水合氨、氢氧化铁等,据此对各选项进行判断.
解答:
解:A.A.醋酸为弱电解质,应写成化学式,不能用H++OH-=H2O表示,故A错误;
B.氨水与盐酸反应,是强酸和弱碱反应生成可溶于水的盐和水,一水合氨不能拆开,不能用离子方程式H++OH-=H2O表示,故B错误;
C.硫酸氢钠与氢氧化钾溶液反应,硫酸氢钠为强电解质,完全电离出氢离子,反应的离子方程式为:H++OH-=H2O,故C正确;
D.氢氧化铁为难溶物,离子方程式中氢氧化铁不能拆开,氢氧化铁与硫酸的反应不能用离子方程式H++OH-=H2O表示,故D错误;
故选C.
B.氨水与盐酸反应,是强酸和弱碱反应生成可溶于水的盐和水,一水合氨不能拆开,不能用离子方程式H++OH-=H2O表示,故B错误;
C.硫酸氢钠与氢氧化钾溶液反应,硫酸氢钠为强电解质,完全电离出氢离子,反应的离子方程式为:H++OH-=H2O,故C正确;
D.氢氧化铁为难溶物,离子方程式中氢氧化铁不能拆开,氢氧化铁与硫酸的反应不能用离子方程式H++OH-=H2O表示,故D错误;
故选C.
点评:本题考查离子方程式的书写,题目难度不大,注意书写离子方程式时,弱电解质和难溶物应写成化学式,明确离子方程式表示的意义为解答关键.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
下列离子方程式书写正确的是( )
| A、CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓ |
| B、澄清石灰水与稀盐酸反应:OH-+H+=H2O |
| C、NaHSO3溶液与NaHSO4溶液混合:SO32-+2H+=H2O+SO2↑ |
| D、铁钉放入硫酸铜溶液中:Fe+3Cu2+=2Fe3++3Cu |
已知①NH3(g)+HCl(g)═NH4Cl(s)?△H 1=-176kJ?mol-1
②NH3(g
NH3(aq)?△H 2=-35.1kJ?mol-1
③HCl(g)
HCl(aq)?△H 3=-72.3kJ?mol-1
④NH3(aq)+HCl(aq)═NH4Cl(aq)?△H 4=-52.3kJ?mol-1
⑤NH4Cl(s)
NH4Cl(aq)?△H 5
则第⑤个反应方程式中的△H5为( )(单位为 kJ?mol-1)
②NH3(g
| ||
③HCl(g)
| ||
④NH3(aq)+HCl(aq)═NH4Cl(aq)?△H 4=-52.3kJ?mol-1
⑤NH4Cl(s)
| ||
则第⑤个反应方程式中的△H5为( )(单位为 kJ?mol-1)
| A、+335.7 |
| B、-335.7 |
| C、+16.3 |
| D、-16.3 |
常温常压时,燃烧23g乙醇(液态),生成二氧化碳气体和液态水,放出的热量为Q,则乙醇燃烧热化学方程式书写正确的是( )
| A、C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-Q | ||||||
B、C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-
| ||||||
C、
| ||||||
| D、C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-2Q |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、7.8g 由Na2S和Na2O2组成的混合物中含有阴离子的数目为 0.1NA |
| B、0.1molAlCl3完全转化为胶体,生成胶体粒子的数目0.l NA个 |
| C、标准状况下,22.4 L乙醇中含有分子的数目为NA |
| D、在过氧化钠与水的反应中,每生成0.1mol 氧气,转移电子的数目为0.4 NA |
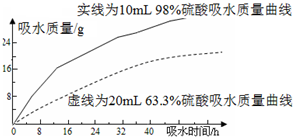 探究浓硫酸的吸水性.某同学把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,根据室温环境下实验的数据绘成的曲线如图.由如图曲线你能得到的实验结论有哪些?(写两点)
探究浓硫酸的吸水性.某同学把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,根据室温环境下实验的数据绘成的曲线如图.由如图曲线你能得到的实验结论有哪些?(写两点)