题目内容
12.我国南方某些地方的井水拿来久置后,井水由澄清透明变为有少量棕红色絮状沉淀积于缸底,水面浮着一层“锈皮”,当地居民采用加明矾的方法处理.(1)井水久置后,水面浮着一层“锈皮”的主要成分是(写化学式)Fe(OH)3
(2)用化学方法除去该井水中主要杂质离子元素所用的试剂(名称)是明矾,离子方程式是Al3++3H2O?Al(OH)3(胶体)+3H+
(3)用化学方法鉴别杂质离子是否除净的方法是滴加KSCN看是否产生血红色.
分析 (1)根据Fe3+水解生成氢氧化铁胶体呈棕红色判断;
(2)明矾中的Al3+水解生成氢氧化铝胶体,胶体具有强的吸附性;
(3)Fe3+遇到KSCN,溶液变成红色.
解答 解:(1)Fe3+水解生成氢氧化铁胶体呈棕红色,故水面浮着的一层“锈皮”为Fe3+水解生成的氢氧化铁胶体,故答案为:Fe(OH)3;
(2)明矾中的Al3+水解生成氢氧化铝胶体,胶体具有强的吸附性,能吸附水中的杂质,其离子方程式为:Al3++3H2O?Al(OH)3(胶体)+3H+,
故答案为:明矾;Al3++3H2O?Al(OH)3(胶体)+3H+;
(3)Fe3+遇到KSCN,溶液变成红色,如果加入KSCN溶液变红说明未经处理,否则已经处理,故答案为:滴加KSCN看是否产生血红色.
点评 本题考查了Fe3+的检验、Fe3+的水解以及明矾的净水作用,难度不大.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
2.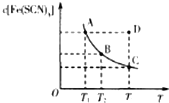 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )| A. | A点与B点相比,A点的血红色沉淀更多 | |
| B. | 加入KCl固体可以使溶液由D点变到C点 | |
| C. | 反应处于D点时,一定有V(正)<V(逆) | |
| D. | 若T1、T2温度下的平衡常数分别为K1、K2,K1<K2 |
20.不溶于水且比水轻的一组液体是( )
| A. | 甲苯、四氯化碳 | B. | 苯、汽油 | C. | 硝基苯、一氯丙烷 | D. | 酒精、溴 |
17.下列说法正确的是( )
| A. | 灼烧某白色粉末,火焰呈黄色,证明原粉末中含有Na+,无K+ | |
| B. | 实验中要配制500mL0.2mol•L-1KCl溶液,需用托盘天平称量7.45gKCl固体 | |
| C. | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,证明NH4Cl固体易升华 | |
| D. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加沸石 |
4.如图所示装置,密闭容器内分别充入空气(已知空气体积占整个容器容积的$\frac{1}{4}$)和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )

| A. | 2:7或5:4 | B. | 2:1或5:4 | C. | 4:5或7:2 | D. | 2:1或7:2 |
1.最简式相同,既不是同系物,又不是同分异构体的是( )
| A. | 乙烯和1-丁烯 | B. | 苯和乙炔 | ||
| C. | 正丁烷和2-甲基丙烷 | D. | 甲苯和乙苯 |
2.1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
| A. | C2H2 | B. | C3H4 | C. | C3H8 | D. | C4H6 |
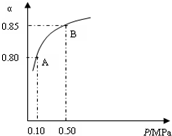 二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.