题目内容
 为了探索外界条件对反应aX(g)+bY(g)?cZ(g)的影响,以X和Y物质的量之比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
为了探索外界条件对反应aX(g)+bY(g)?cZ(g)的影响,以X和Y物质的量之比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )| A、△H>0 a+b>c |
| B、△H<0 a+b<c |
| C、△H<0 a+b>c |
| D、△H>0 a+b<c |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:根据图象判断温度、压强变化Z的物质的量分数的变化趋势,以此温度、压强对平衡移动的影响,可得出反应热以及反应前后化学计量数关系.
解答:
解:由图象可知,降低温度,Z的物质的量分数增大,说明降低温度平衡向正反应方向移动,说明正反应放热,则△H<0,
降低压强,Z的物质的量分数减小,说明压强减小,平衡向你反应方向移动,则应有a+b>c,
故选C.
降低压强,Z的物质的量分数减小,说明压强减小,平衡向你反应方向移动,则应有a+b>c,
故选C.
点评:本题考查温度、压强等外界条件对平衡移动的影响,题目难度中等,解答本题的关键是能正确分析图象曲线的变化趋势.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组中的两种物质作用时,反应条件(温度、反应物用量、浓度)改变,不会引起产物种类改变的是( )
| A、Fe和Cl2 |
| B、NaOH和SO2 |
| C、Na和O2 |
| D、C和O2 |
利用电解原理,在铁皮表面镀一层锌的有关叙述正确的是( )
| A、铁为负极,锌为正极 |
| B、铁为阳极,锌为阴极 |
| C、用可溶性铁盐作电解液 |
| D、锌元素既被氧化又被还原 |
下列有关铜锌原电池的叙述正确的是( )
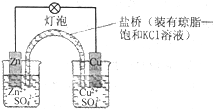

| A、盐桥中的Cl-移向CuSO4溶液 |
| B、电池总反应为Zn+Cu2+=Zn2++Cu |
| C、在外电路中,电子从正极流向负极 |
| D、取下盐桥,原电池仍可工作 |
下列物质中,碱性最强的是( )
| A、Mg(OH)2 |
| B、NaOH |
| C、KOH |
| D、LiOH |
下列物质中,含有的分子数目最少的是( )
| A、0.5molCO2 |
| B、标准状况下11.2L氨气 |
| C、8 g水 |
| D、6.02×1023个氯分子 |
设阿伏加德罗常数(NA)的数值为nA,下列说法中正确的是( )
| A、1 mol Cl2与足量NaOH反应,转移的电子数为2nA |
| B、1 mo1Na被完全氧化生成Na2O2,失去的电子数为2nA |
| C、常温常压下,22.4LSO2气体中含有的原子数小于3nA |
| D、0.1 mol/LNaOH溶液中含有Na+的数目为0.1 nA |

