题目内容
18.下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或者化学式填空回答:| 族 周期 | IA | IIA | ⅢA | ⅣA | VA | VIA | VIIA | 0 |
| ① | ② | ③ | ||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 ;
;(2)元素最高价氧化物对应水化物中,酸性最强的是HClO4(填酸的化学式,下同)碱性最强的是NaOH;呈现两性的是Al(OH)3;写出三者之间相互反应的化学方程式H++OH-=H2O;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)元素②③④⑤离子半径由大到小的顺序是O2->F->Na+>Mg2+;
(4)元素①的最高价氧化物的水化物的稀溶液与铜反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(5)元素①和⑨的氢化物之间反应的化学方程式为NH3+HCl=NH4Cl;
(6)元素③和⑨的氢化物的酸性强弱顺序为HCl>HF.
分析 由元素在周期表中的位置可知,①为N,②为O,③为F,④为Na,⑤为Mg,⑥为Al,⑦为Si,⑧为S,⑨为Cl,⑩为Ar,
(1)在这些元素中,可以做半导体材料的是Si,化学性质最不活泼的为稀有气体元素Ar;
(2)元素金属性越强其最高价氧化物对应水化物碱性越强,元素非金属性越强其最高价氧化物对应水化物酸性越强;
(3)电子层越多半径越大,电子层一样多的原子,核电荷数越多半径越小;
(4)Cu与元素①的最高价氧化物的水化物的稀溶液反应,生成硝酸铜、NO和水;
(5)元素①和⑨的氢化物属于氨气和氯化氢气体,二者反应生成氯化铵;
(6)元素③和⑨的氢化物分别是HF和HCl,HF属于弱酸,HCl属于强酸.
解答 解:由元素在周期表中的位置可知,①为N,②为O,③为F,④为Na,⑤为Mg,⑥为Al,⑦为Si,⑧为S,⑨为Cl,⑩为Ar,
(1)以上元素中可以做半导体材料的是Si,而只有Ar的最外层电子数为8,性质不活泼,最稳定,其原子结构示意图为 ,故答案为:Si,
,故答案为:Si, ;
;
(2)以上元素中最高价氧化物对应的水化物中酸性最强的为HClO4,碱性最强的为NaOH,呈两性的氢氧化物为Al(OH)3,故答案为:HClO4;NaOH;Al(OH)3;
氢氧化钠与高氯酸反应生成高氯酸钠和水,离子方程式:H++OH-=H2O;
氢氧化铝与高氯酸反应生成高氯酸铝和水,离子方程式:Al(OH)3+3H+=Al3++3H2O;
氢氧化钠与氢氧化铝反应生成偏铝酸钠和水,离子方程式:Al(OH)3+OH-=AlO2-+2H2O;
故答案为:HClO4;NaOH;Al(OH)3;H++OH-=H2O;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)电子层一样多的原子,核电荷数越多半径越小,O2-、F-、Na+、Mg2+均为10电子离子,故半径O2->F->Na+>Mg2+,故答案为:O2->F->Na+>Mg2+;
(4)Cu与元素①的最高价氧化物的水化物的稀溶液反应,生成硝酸铜、NO和水,反应为3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(5)元素①和⑨的氢化物属于氨气和氯化氢气体,二者反应生成氯化铵,反应的化学方程式为NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
(6)元素③和⑨的氢化物分别是HF和HCl,H-F键能大于H-Cl键能,故H-F与H-Cl相比不易断裂,即电离出氢离子的能力弱,HF属于弱酸,HCl属于强酸,故答案为:HCl>HF.
点评 本题考查元素周期表和元素周期律,熟悉元素在周期表中的位置是解答本题的关键,难度不大,注意化学用语的使用来解答.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案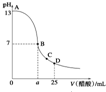 25℃时,在25mL 0.1mol•L-1的NaOH溶液中,逐滴加入0.2mol•L -1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析不正确的是( )
25℃时,在25mL 0.1mol•L-1的NaOH溶液中,逐滴加入0.2mol•L -1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析不正确的是( )| A. | B点的横坐标a>12.5 | |
| B. | C点时溶液中有:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | D点时溶液中有:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| D. | 曲线上A、B间的任意一点,溶液中都有:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| A. | 该元素位于元素周期表的第三周期ⅦA族 | |
| B. | 生成的盐含有的化学键既有离子键又有共价键 | |
| C. | 该元素的常见化合价有:-1、0、+1、+3、+5、+7等 | |
| D. | 该元素的氢化物的稳定性比PH3、H2S弱 |
| A. | 半径:Y2->Z->X+>W3+ | B. | 还原性:Y2->Z- | ||
| C. | 氧化性:W3+>X+ | D. | 质子数:c>d>b>a |
| A. | 28 g C2H4所含共用电子对数目为4NA | |
| B. | 1 L 0.1 mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 1 mol甲烷分子所含质子数为10NA | |
| D. | 标准状况下,22.4 L乙醇的分子数为NA |
【查阅资料】
①CuSO4与Na2SO3溶液混合可制备Cu2O.
②Cu2O为砖红色固体;酸性条件下生成Cu2+和Cu.
③Cu2O和Cu(SO3)23-可以相互转化
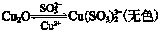
(1)配制0.25mol•L-1CuSO4溶液和0.25mol•L-1 Na2SO3溶液.测得CuSO4溶液pH=4,Na2SO3溶液pH=9.用离子方程式表示CuSO4溶液pH=4的原因Cu2++2H2O?Cu(OH)2+2H+.
(2)完成CuSO4溶液和Na2SO3溶液反应制Cu2O的离子方程式:
□Cu2++□SO32-+□2H2O $\frac{\underline{\;\;△\;\;}}{\;}$□Cu2O↓+□SO42-+□HSO3-
【实验探究】
| 操作 | 现象 |
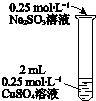 | i 有黄色沉淀出现,随着 Na2SO3溶液的滴入,沉淀增加,当加到5mL时,溶液的蓝色消失. ii 将试管加热,黄色沉淀变为砖红色,有刺激性气味气体产生. iii在加热条件下,继续滴入Na2SO3溶液,砖红色沉淀减少,当1加到10mL时,沉淀完全溶解,得无色溶液. |
(4)经检验 i中黄色沉淀含有Cu2SO3,ii中沉淀由黄色变砖红色的化学方程式是Cu2SO3═Cu2O+SO2↑.
(5)iii中砖红色沉淀消失的原因是Cu2O转化得无色Cu(SO3)23-.
(6)在加热条件下,若向2mL 0.25mol•L-1Na2SO3溶液中滴加0.25mol•L-1CuSO4溶液至
过量,预期观察到的现象是产生砖红色沉淀,且沉淀不消失.
(7)由上述实验得出结论:CuSO4溶液和Na2SO3溶液反应制备Cu2O,应控制的条件是
反应温度、CuSO4和Na2SO3的物质的量之比.