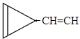
题目内容
8.某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.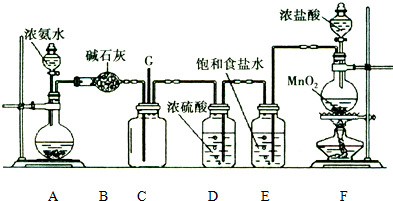
请回答下列问题:
(1)装置F中发生反应的离子方程式为MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O.
(2)装置A的烧瓶中可装试剂碱石灰或生石灰等.
分析 (1)F中二氧化锰和浓盐酸反应制备氯气,二者在加热条件下反应生成氯气、氯化锰和水;
(2)碱石灰具有吸水性,利用碱石灰与浓氨水可制取氨气.
解答 解:(1)二氧化锰和浓盐酸在加热条件下反应生成氯气、氯化锰和水,离子方程式:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O;
故答案为:MnO2+4H++2C1-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++C12↑+2H2O;
(2)碱石灰或生石灰等与浓氨水混合可制取氨气,所以装置A的烧瓶中可装试剂为碱石灰或生石灰等;
故答案为:碱石灰或生石灰等.
点评 本题考查了氨气、氯气的制备实验,题目难度不大,侧重于实验原理和试剂选择的考查,注意把握实验室制备氯气的反应原理.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
18.下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或者化学式填空回答:
(1)在这些元素中,可以做半导体材料的是Si,化学性质最不活泼的原子结构示意图为 ;
;
(2)元素最高价氧化物对应水化物中,酸性最强的是HClO4(填酸的化学式,下同)碱性最强的是NaOH;呈现两性的是Al(OH)3;写出三者之间相互反应的化学方程式H++OH-=H2O;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)元素②③④⑤离子半径由大到小的顺序是O2->F->Na+>Mg2+;
(4)元素①的最高价氧化物的水化物的稀溶液与铜反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(5)元素①和⑨的氢化物之间反应的化学方程式为NH3+HCl=NH4Cl;
(6)元素③和⑨的氢化物的酸性强弱顺序为HCl>HF.
| 族 周期 | IA | IIA | ⅢA | ⅣA | VA | VIA | VIIA | 0 |
| ① | ② | ③ | ||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 ;
;(2)元素最高价氧化物对应水化物中,酸性最强的是HClO4(填酸的化学式,下同)碱性最强的是NaOH;呈现两性的是Al(OH)3;写出三者之间相互反应的化学方程式H++OH-=H2O;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)元素②③④⑤离子半径由大到小的顺序是O2->F->Na+>Mg2+;
(4)元素①的最高价氧化物的水化物的稀溶液与铜反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(5)元素①和⑨的氢化物之间反应的化学方程式为NH3+HCl=NH4Cl;
(6)元素③和⑨的氢化物的酸性强弱顺序为HCl>HF.
19.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 104 | 66 |
| 主要化合价 | +2 | +3 | +6、+4、-2 | -2 |
| A. | X、Y元素的金属性X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW3 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
16.下列物质可用来鉴别乙酸、乙醇和苯的是( )
| A. | 澄清石灰水 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 紫色石蕊试液 |
3.W、X、Y、Z均为短周期元素,W-的电子层结构与氦相同,X、Y处在同一周期,X、Y的原子最外层电子数分别为1、6,Z原子的L电子层有7个电子,下列说法正确的是( )
| A. | 单质沸点:W>Z | |
| B. | 离子半径:Y2->Z- | |
| C. | 原子序数:Z>Y>X>W | |
| D. | W分别与Y、Z形成的化合物中均只含极性共价键 |
1.一定温度下,向某容积为VL的密闭容器中充入amolA和bmolB,发生反应:aA(g)+bB(s)?cC(g);5min时,测得C为xmol.下列说法中一定正确的是( )
| A. | 5min时,v(C)=$\frac{x}{5}$Vmol•L-1•s-1 | |
| B. | 缩小容器体积平衡一定发生移动 | |
| C. | 0-5min内,v(A):v(C)=a:c | |
| D. | 0-5min内,用A表示的反应速率为$\frac{xc}{300aV}$mol•L-1•s-1 |
 ⑤
⑤
 _.
_. D.
D. E.
E.