题目内容
8.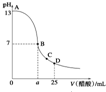 25℃时,在25mL 0.1mol•L-1的NaOH溶液中,逐滴加入0.2mol•L -1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析不正确的是( )
25℃时,在25mL 0.1mol•L-1的NaOH溶液中,逐滴加入0.2mol•L -1的CH3COOH溶液,溶液的pH与醋酸体积关系如图所示,下列分析不正确的是( )| A. | B点的横坐标a>12.5 | |
| B. | C点时溶液中有:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | D点时溶液中有:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| D. | 曲线上A、B间的任意一点,溶液中都有:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
分析 A.醋酸钠是强碱弱酸盐,其水溶液呈碱性,要使混合溶液呈中性,则醋酸应该稍微过量;
B.C点溶液呈酸性,则c(H+)>c(OH-),且溶液中溶质为醋酸和醋酸钠,醋酸电离程度大于醋酸根离子水解程度而导致溶液呈酸性,根据电荷守恒判断;
C.D点溶液中溶质为等物质的量浓度的醋酸钠和醋酸,溶液中存在物料守恒;
D.溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒判断.
解答 解:A.醋酸钠是强碱弱酸盐,其水溶液呈碱性,要使混合溶液呈中性,则醋酸应该稍微过量,所以B点的横坐标a>12.5,故A正确;
B.C点溶液呈酸性,则c(H+)>c(OH-),且溶液中溶质为醋酸和醋酸钠,醋酸电离程度大于醋酸根离子水解程度而导致溶液呈酸性,根据电荷守恒得c(CH3COO-)>c(Na+),醋酸电离程度较小,所以c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故B正确;
C.D点溶液中溶质为等物质的量浓度的醋酸钠和醋酸,溶液中存在物料守恒,根据物料守恒得c(CH3COO-)+c(CH3COOH)=2c(Na+),故C正确;
D.溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒得c(CH3COO-)<c(Na+),如果醋酸浓度很小,还存在c(CH3COO-)<c(OH-),故D错误;
故选D.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生识图及判断能力,明确曲线上点所对应溶液中的溶质成分及其性质是解本题关键,知道溶液中存在的电荷守恒和物料守恒,题目难度不大.

练习册系列答案
相关题目
16.在密闭容器中加入2.0mol SO2和1.0mol O2,一定条件下发生如下反应2SO2+O2?2SO3.反应达到平衡后,各物质的物质的量可能为( )
| n(SO2)/mol | n(O2)/mol | n(SO3)/mol | |
| A | 2.0 | 1.0 | 0 |
| B | 1.0 | 0 | 1.0 |
| C | 0.20 | 0.10 | 1.80 |
| D | 0 | 0 | 2.0 |
| A. | A | B. | B | C. | C | D. | D |
3.1kg物质的量浓度为16.8mol/L,质量分数为88%的浓硫酸,与1L水混合后,得到质量分数为44%的稀硫酸,该稀硫酸的物质的量浓度可能为( )
| A. | =8.4 | B. | >8.4 | C. | <8.4 | D. | ≤8.4 |
20.有CH3OH、CH3COOH和丙三醇(C3H8O3)组成的混合液体,其中碳的质量分数39%,则氢的质量分数为( )
| A. | 6.7% | B. | 8.7% | C. | 9% | D. | 12.5% |
18.下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或者化学式填空回答:
(1)在这些元素中,可以做半导体材料的是Si,化学性质最不活泼的原子结构示意图为 ;
;
(2)元素最高价氧化物对应水化物中,酸性最强的是HClO4(填酸的化学式,下同)碱性最强的是NaOH;呈现两性的是Al(OH)3;写出三者之间相互反应的化学方程式H++OH-=H2O;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)元素②③④⑤离子半径由大到小的顺序是O2->F->Na+>Mg2+;
(4)元素①的最高价氧化物的水化物的稀溶液与铜反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(5)元素①和⑨的氢化物之间反应的化学方程式为NH3+HCl=NH4Cl;
(6)元素③和⑨的氢化物的酸性强弱顺序为HCl>HF.
| 族 周期 | IA | IIA | ⅢA | ⅣA | VA | VIA | VIIA | 0 |
| ① | ② | ③ | ||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 ;
;(2)元素最高价氧化物对应水化物中,酸性最强的是HClO4(填酸的化学式,下同)碱性最强的是NaOH;呈现两性的是Al(OH)3;写出三者之间相互反应的化学方程式H++OH-=H2O;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)元素②③④⑤离子半径由大到小的顺序是O2->F->Na+>Mg2+;
(4)元素①的最高价氧化物的水化物的稀溶液与铜反应的化学方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(5)元素①和⑨的氢化物之间反应的化学方程式为NH3+HCl=NH4Cl;
(6)元素③和⑨的氢化物的酸性强弱顺序为HCl>HF.
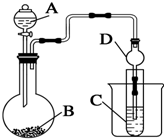 某兴趣小组设计如下实验来证明同周期元素Cl和S的非金属性强弱.
某兴趣小组设计如下实验来证明同周期元素Cl和S的非金属性强弱. ;Na2O2
;Na2O2 ; CO2
; CO2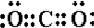 .
.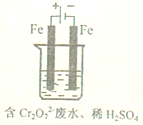 工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.常用的处理方法有两种.