题目内容
20.设NA为阿伏加德罗常数,下列有关叙述正确的是( )| A. | 1molSO2与0.5molO2反应生成的SO3分子数为NA | |
| B. | 标准状况下,11.2LHF中含有的共价键为0.5NA | |
| C. | 1L 0.5mol/LCH3COOH溶液中含有的H+数大于0.5NA | |
| D. | 一定量的铁与1mol氯气恰好完全反应,转移电子数为2NA |
分析 A、二氧化硫和氧气的反应为可逆反应;
B、标况下HF为液体;
C、醋酸是弱电解质,不能完全电离;
D、氯气反应后变为-1价.
解答 解:A、二氧化硫和氧气的反应为可逆反应,不能进行彻底,生成的SO3分子数为NA,故A错误;
B、标况下HF为液体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、醋酸是弱电解质,不能完全电离,故溶液中的氢离子的个数小于0.5NA个,故C错误;
D、氯气反应后变为-1价,故1mol氯气转移2NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.化学与生活、社会密切相关,下列说法不正确的是( )
| A. | 煤、石油、天然气属于化石能源,太阳能、氢能、风能、地热能、海洋能属于新能源 | |
| B. | 白铁(镀锌铁板)比马口铁(镀锡铁板)更耐腐蚀 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应采取深度填埋法 | |
| D. | 测试和调控溶液的pH对工农业生产、科学研究及日常生活和医疗保健都有重要意义 |
15.化学与生活、生产密切相关,下列有关叙述正确的是( )
| A. | 氢氧化铝、小苏打、纯碱均可用作胃酸中和剂 | |
| B. | 古代的陶瓷、水泥、石英玻璃等,都是硅酸盐产品 | |
| C. | 将草木灰(含K2CO3)与NH4Cl混合使用会降低肥效 | |
| D. | 石油的分馏、煤的干馏等物理变化在生产中有着重要的地位 |
5.为了提纯下列物质(括号内为杂质),所选用的除杂试剂、分离方法、必用仪器均正确的是( )
| 选项 | 不纯物质(杂质) | 除杂试剂或分离方法 | 必用仪器 |
| A | 碘水 | 酒精、萃取 | 分液漏斗 |
| B | 二氧化碳(一氧化碳) | 点燃 | |
| C | 硝酸钾(氯化钠) | 直接蒸发结晶 | 蒸发皿 |
| D | 乙醇(水) | 生石灰、蒸馏 | 蒸馏烧瓶 |
| A. | A | B. | B | C. | C | D. | D |
12.下列实验操作和数据记录都正确的是( )
| A. | 用25 mL碱式滴定管量取高锰酸钾溶液,体积为16.60 mL | |
| B. | 用标准NaOH溶液滴定未知浓度盐酸,用去NaOH溶液20.50 mL | |
| C. | 用10 mL量筒量取8.25 mL盐酸 | |
| D. | 用pH试纸测得某溶液pH为3.2 |
9.等物质的量浓度、等体积的酸HA与碱NaOH 溶液混合后,溶液的酸碱性是( )
| A. | 酸性 | B. | 中性 | C. | 碱性 | D. | 前三者都有可能 |
10.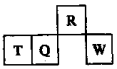 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中W所处的周期序数是最外层电子数的一半.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中W所处的周期序数是最外层电子数的一半.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中W所处的周期序数是最外层电子数的一半.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中W所处的周期序数是最外层电子数的一半.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 含T的盐溶液一定显酸性 | |
| D. | 实验室制备T的氢氧化物可以通过R形成的氢化物通入到T离子的溶液中得到 |
