题目内容
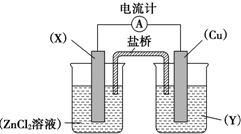 依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.
依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.请回答下列问题:
(1)电极X的材料是
(2)铜电极为电池的
(3)外电路中的电子是从
(4)盐桥中的Cl-向
考点:原电池和电解池的工作原理
专题:电化学专题
分析:由反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)可知,Zn元素化合价升高,被氧化,Cu元素化合价降低,被还原,形成原电池知识时,Zn为负极,由图可知,Cu为正极,Y为氯化铜溶液,以此解答该题.
解答:
解:(1)由反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)可知,Zn元素化合价升高,被氧化,应为负极,正极为铜,则电解质溶液Y为CuCl2,
故答案为:Zn;CuCl2;
(2)铜为正极,电极反应为 Cu2++2e-=Cu,X为负极,电极反应为Zn-2e-=Zn2+,
故答案为:正;Cu2++2e-=Cu;
(3)原电池工作时,电子由负极经导线流向正极,即由Zn流向Cu,
故答案为:Zn;Cu;
(4)原电池工作时,阴离子向负极移动,如将盐桥撤掉,不能形成闭合回路,电流计的指针不偏转,
故答案为:Zn;不.
故答案为:Zn;CuCl2;
(2)铜为正极,电极反应为 Cu2++2e-=Cu,X为负极,电极反应为Zn-2e-=Zn2+,
故答案为:正;Cu2++2e-=Cu;
(3)原电池工作时,电子由负极经导线流向正极,即由Zn流向Cu,
故答案为:Zn;Cu;
(4)原电池工作时,阴离子向负极移动,如将盐桥撤掉,不能形成闭合回路,电流计的指针不偏转,
故答案为:Zn;不.
点评:本题考查原电池的设计及工作原理,注意电极反应式的书写方法,牢固掌握原电池中电极的判断,电极反应式的书写的方法性问题.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列溶液中各粒子的浓度关系不正确的是( )
| A、0.1 mol/L HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
| B、0.1 mol/L CuSO4?(NH4)2SO4?6H2O溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| C、0.1 mol/L NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)>c(HCO3-)+c(CO32-)+c(OH-) |
| D、等物质的量的NaX和弱酸HX混合后溶液中:c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
 如图所示为条件一定时,反应2NO(g)+O2(g)?2NO2(g) (正反应为放
如图所示为条件一定时,反应2NO(g)+O2(g)?2NO2(g) (正反应为放热)中NO的转化率与温度变化关系曲线图,图中有a、b、c、d四个点,其中表示未达到平衡状态,且v正<v逆的点是( )
| A、a | B、b | C、c | D、d |
下列有关硅及其化合物的说法错误的是( )
| A、硅的导电性能介于导体和绝缘体之间,是良好的半导体材料 |
| B、二氧化硅属于酸性氧化物,不能与任何酸反应 |
| C、硅酸可通过可溶性硅酸盐与其他酸反应制得,硅酸干凝胶常用作干燥剂 |
| D、硅酸钠的水溶液俗称水玻璃,可作木材防火剂 |
下列反应中必须加入氧化剂才能进行的是( )
| A、Fe2+→Fe3+ |
| B、CO32-→CO2 |
| C、SO32-→HSO3- |
| D、MnO4-→Mn2+ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0 mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、pH<5的溶液:NH4+、Na+、S2-、Cl- |
| C、pH=12的溶液:K+、Na+、CH3COO-、Br- |
| D、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A、泥水 | B、淀粉溶液 |
| C、蒸馏水 | D、稀硫酸 |