题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0 mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、pH<5的溶液:NH4+、Na+、S2-、Cl- |
| C、pH=12的溶液:K+、Na+、CH3COO-、Br- |
| D、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
考点:离子共存问题
专题:
分析:A.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子;
B.pH<5的为酸性溶液,硫离子能够与氢离子反应生成硫化氢;
C.pH=12的溶液中存在大量氢氧根离子,K+、Na+、CH3COO-、Br-之间不发生反应,都不与氢氧根离子反应;
D.与铝反应生成氢气的溶液为酸性或强碱性溶液,酸性溶液中,碳酸根离子与氢离子反应.
B.pH<5的为酸性溶液,硫离子能够与氢离子反应生成硫化氢;
C.pH=12的溶液中存在大量氢氧根离子,K+、Na+、CH3COO-、Br-之间不发生反应,都不与氢氧根离子反应;
D.与铝反应生成氢气的溶液为酸性或强碱性溶液,酸性溶液中,碳酸根离子与氢离子反应.
解答:
解:A.硝酸钾与H+、Fe2+之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.pH<5的溶液为酸性溶液,S2-与氢离子反应,在溶液中不能大量共存,故B错误;
C.pH=12的溶液中存在大量氢氧根离子,K+、Na+、CH3COO-、Br-之间不反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.与铝反应生成氢气的溶液中存在大量氢离子或氢氧根离子,酸性溶液中,CO32-与氢离子反应,在溶液中不能大量共存,故D错误;
故选C.
B.pH<5的溶液为酸性溶液,S2-与氢离子反应,在溶液中不能大量共存,故B错误;
C.pH=12的溶液中存在大量氢氧根离子,K+、Na+、CH3COO-、Br-之间不反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.与铝反应生成氢气的溶液中存在大量氢离子或氢氧根离子,酸性溶液中,CO32-与氢离子反应,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
在pH为4-5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀.工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解.欲除去溶液中的杂质离子,下述方法正确的是( )
| A、加入纯Cu将Fe2+还原 |
| B、向溶液中加入(NH4)2S使Fe2+沉淀 |
| C、直接加水加热使杂质离子水解除去 |
| D、在溶液中通入Cl2,再加入CuO粉末调节pH为4-5 |
将22.6克Mg、Al、Fe溶于过量的1LpH=0的硫酸溶液中,然后向其中加入氢氧化钠溶液使Mg2+、Al3+、Fe2+刚好完全沉淀,用掉氢氧化钠溶液1升,则氢氧化钠溶液的浓度是( )
| A、1mol/L |
| B、2mol/L |
| C、3mol/L |
| D、0.5mol/L |
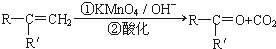 (R、R'可表示烃基或官能团)
(R、R'可表示烃基或官能团)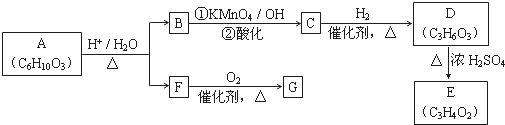
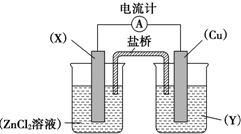 依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.
依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.