题目内容
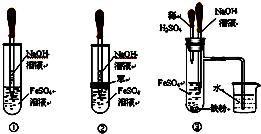
10. 用下面两种方法均可制得Fe(OH)2白色沉淀.
用下面两种方法均可制得Fe(OH)2白色沉淀.方法一:用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备.
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入稀H2SO4;铁屑.
(2)除去蒸馏水中溶解的O2常采用加热煮沸的方法.
(3)制取Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是:防止发生反应4Fe(OH)2+O2+2H2O=4Fe(OH)3.(填化学方程式)
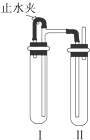
方法二 在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备.
(4)在试管Ⅰ里加入的试剂是稀H2SO4、铁屑.
(5)为了制得Fe(OH)2白色沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是检验试管Ⅱ出口处排出的氢气的纯度.当排出的H2纯净时,再夹紧止水夹.
分析 (1)根据FeSO4易被空气中的氧气氧化和易水解的特点分析;
(2)根据气体的溶解度随温度的升高而减小分析;
(3)根据氢氧化亚铁极易被空气中的氧气氧化成氢氧化铁分析;
(4)根据铁屑与稀H2SO4反应生成硫酸亚铁溶液;
(5)打开止水夹,Fe与H2SO4反应生成H2充满整个装置,反应一段时间后关闭止水夹,左侧试管内气压升高,反应生成的Fe2+沿导管进入右侧试管与NaOH反应生成白色沉淀Fe(OH)2.
解答 解:(1)根据FeSO4具有易被氧化和易水解的特点,在配制其溶液时还需加入稀H2SO4防止 发生水解反应,同时加入铁屑防止硫酸亚铁被氧化.
故答案为:稀H2SO4;铁屑;
(2)蒸馏水中若溶有O2,则会加速Fe(OH)2氧化,由于氧气的溶解度随温度的升高而减小,因此可采用加热煮沸的方法除去.
故答案为:加热煮沸;
(3)用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,是为避免生成的Fe(OH)2沉淀接触O2,发生反应的方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)铁与硫酸反应生成氢气,关闭止水夹,会使装置Ι中压强变大,使Ι中的药品进入Ⅱ中,与Ⅱ中的药品反应得到氢氧化亚铁,所以在试管I里加入试剂稀H2SO4、铁屑,获得硫酸亚铁溶液,故答案为:稀H2SO4、铁屑;
(5)打开止水夹,Fe与H2SO4反应生成H2充满整个装置,反应一段时间后关闭止水夹,左侧试管内气压升高,反应生成的Fe2+沿导管进入右侧试管与NaOH反应生成白色沉淀Fe(OH)2.若过早关闭止水夹,使左侧试管中的硫酸压入右侧试管中,将NaOH中和,则得不到Fe(OH)2溶液,故答案为:检验试管Ⅱ出口处排出的氢气的纯度,当排出的H2纯净时,再夹紧止水夹.
点评 Fe(OH)2很容易被空气中的氧气氧化,这是Fe(OH)2的重要性质,本题是在原有性质基础上进行了改编,设计成了探究型实验题,此题考查的内容比较多,既有水解方面的问题,又有氧化还原方面的问题,还有实验中的实际问题,同时还考查了实验的设计,可以说是一道不可多得的好题.

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案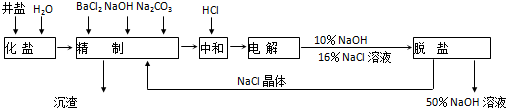
依据如图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极的电极反应式为2Cl--2e-=Cl2↑;
(2)电解过程的总反应的化学方程式2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(3)电解槽阳极产物可用于制漂白粉、生产盐酸、自来水消毒、制高纯硅、合成塑料等(任写2种)(至少写出两种用途).
(4)工业食盐含Ca2+、Mg2+等杂质,精制过程中除去这2种离子所发生反应的离子方程式为:Ca2++CO32-=CaCO3↓、Mg2++2OH-=Mg(OH)2↓.
(5)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是a、c
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(6)为了有效除去Ca2+、Mg2+、SO42-加入试剂的合理顺序为b、c
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(7)已知NaOH、NaCl在水中的溶解度数据如下表:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaOH/g | 109 | 118 | 129 | 146 | 177 | 300 | 313 | 318 | 337 |
| NaCl/g | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
| A. | 乙苯和环己烯都能使酸性高锰酸钾溶液褪色 | |
| B. | 糖、油脂、蛋白质都能发生水解反应 | |
| C. | 甲醛和乙二醇都可作为合成高分子化合物的单体 | |
| D. | 丙烷和2-甲基丙烷的一氯代物均为两种 |
| A. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氧化铜溶于硫酸:O2-+2H+═H2O | |
| D. | 碳酸钙溶于醋酸CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ |
| A. | pH=8的氢氧化钠溶液1mL与999mL水混合 | |
| B. | pH=12的氢氧化钠溶液与pH=2的某酸溶液等体积混合 | |
| C. | pH=2的盐酸与0.01mol/L的氨水等体积混合 | |
| D. | 1×10-3mol/L的盐酸和4×10-4mol/L的Ba(OH)2溶液各取10mL,混合后再稀释100倍 |



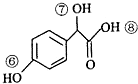 )的说法正确的是AD.
)的说法正确的是AD.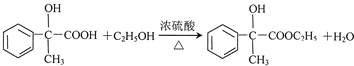 .
.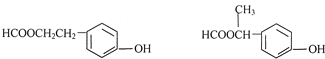 .
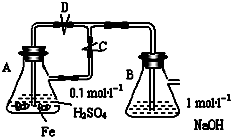
.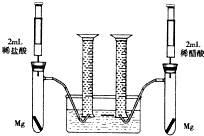 某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图(夹持仪器略):
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图(夹持仪器略):