题目内容
在标准状况下,44.8L HCl的质量是 g,溶于水制成500mL溶液,所得溶液的物质的量浓度为 mol/L,取此溶液10mL,加入0.5mol/L的Ba(OH)2溶液 mL才能正好中和.
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据n=
计算HCl的物质的量,根据m=nM计算HCl的质量,根据c=
计算溶液物质的量浓度,发生反应:Ba(OH)2+2HCl=BaCl2+22O,由方程式可知n(HCl)=2n(Ba(OH)2,进而计算Ba(OH)2溶液的体积.
| V |
| Vm |
| n |
| V |
解答:
解:标况下,44.8L HCl的物质的量=
=2mol,
HCl的质量=2mol×36.5g/mol=73g,
溶于水制成500mL溶液,所得溶液的物质的量浓度为
=4mol/L,
发生反应:Ba(OH)2+2HCl=BaCl2+22O,由方程式可知n(HCl)=2n(Ba(OH)2,令需要氢氧化钡溶液的体积为V,则:10mL×4mol/L=V×0.5mol/L×2,解得V=40mL,
故答案为:73;4;40.
| 44.8L |
| 22.4L/mol |
HCl的质量=2mol×36.5g/mol=73g,
溶于水制成500mL溶液,所得溶液的物质的量浓度为
| 2mol |
| 0.5L |
发生反应:Ba(OH)2+2HCl=BaCl2+22O,由方程式可知n(HCl)=2n(Ba(OH)2,令需要氢氧化钡溶液的体积为V,则:10mL×4mol/L=V×0.5mol/L×2,解得V=40mL,
故答案为:73;4;40.
点评:本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
120℃,某气态烃在密闭容器中与足量的O2混合点燃,完全燃烧后恢复至原温度,容器内的压强保持不变,则该烃是( )
| A、CH4 |
| B、C2H6 |
| C、C3H6 |
| D、C3H8 |
下列反应原理不符合工业冶炼金属实际情况的是( )
A、2HgO
| ||||
B、2NaCl(熔融)
| ||||
C、2MgO(熔融)
| ||||
D、Fe2O3+3CO
|
最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是( )
| A、该晶体类型是原子晶体 |
| B、该晶体中碳原子和氧原子的个数比为1:2 |
| C、每摩尔该晶体中含4molC-O |
| D、晶体的空间最小环共有6个原子构成 |
 的系统命名是:
的系统命名是: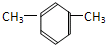 的名称是
的名称是 的系统命名是
的系统命名是