题目内容
相同标准状况下,2g H2与16g O2混合后,其体积为 L,平均相对分子质量为 ,密度为 g/L.
考点:气体摩尔体积
专题:阿伏加德罗常数和阿伏加德罗定律
分析:由n=
求出H2与O2混的物质的量,带入V=nVm计算体积,带入M=
计算平均摩尔质量,代入ρ=
计算密度.
| m |
| M |
| m |
| n |
| m |
| V |
解答:
解:n( H2)=
=1mol,n(O2)=
=0.5mol,混合气体的总物质的量n=1mol+0.5mol=1.5mol,混合气体的体积V=1.5mol×22.4L/mol=33.6L;
混合气体的平均摩尔质量M=
=
=12g/mol,则混合气体平均相对分子质量为12;入ρ=
=
=0.536g/L,
故答案为:33.6;12;0.536.
| 2g |
| 2g/mol |
| 16g |
| 32g/mol |
混合气体的平均摩尔质量M=
| m |
| n |
| 2g+16g |
| 1.5mol |
| m |
| V |
| 2g+16g |
| 33.6L |
故答案为:33.6;12;0.536.
点评:本题考查了以物质的量为中心的计算,题目难度不大,掌握n=
=
、ρ=
公式的正确运算是解题的关键,注意平均相对分子质量通过平均摩尔质量求算.
| m |
| M |
| V |
| Vm |
| m |
| V |

练习册系列答案
相关题目
下列说法正确的是( )
| A、纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖 |
| B、2,3一二甲基丁烷的H一NMR上有5个峰 |
| C、含5个碳原子的有机物,每个分子中最多可形成4个C一C单键 |
D、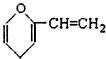 某有机物结构如图所示,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种 |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C2H4 CH4 |
| C、C60 C2H4 |
| D、NH3 HCl |