题目内容
下列关于铜的说法正确的是( )
| A、铜在干燥的空气中和在潮湿的空气中存在的形态相同 |
| B、相同质量的铜分别与足量的氯气、硫完全反应,失去的电子数相同 |
| C、相同物质的量的浓硫酸分别与足量的铜和氧化铜反应,生成硫酸铜的量相同 |
| D、相同质量的铜分别与足量的稀硝酸、浓硝酸完全反应,生成气体的物质的量不同 |
考点:铜金属及其重要化合物的主要性质
专题:几种重要的金属及其化合物
分析:A、Cu在潮湿的空气有铜绿生成,而在干燥的空气中则不会;
B、由于Cu+Cl2=CuCl2,而2Cu+S=Cu2S,显然相同质量的铜参加反应,失去的电子数不相同;
C、浓硫酸与铜发生氧化还原反应;
D、根据Cu与浓、稀HNO3反应的化学方程式可判断生成的NO2和NO的物质的量不相同;
B、由于Cu+Cl2=CuCl2,而2Cu+S=Cu2S,显然相同质量的铜参加反应,失去的电子数不相同;
C、浓硫酸与铜发生氧化还原反应;
D、根据Cu与浓、稀HNO3反应的化学方程式可判断生成的NO2和NO的物质的量不相同;
解答:
解:A.Cu在潮湿的空气有铜绿生成,而在干燥的空气中则不会,故A错误;
B.由于Cu+Cl2=CuCl2,而2Cu+S=Cu2S,显然相同质量的铜参加反应,失去的电子数不相同,故B错误;
C.根据Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,CuO+H2SO4=CuSO4+H2O可知,相同物质的量的H2SO4(浓)参加反应,前者生成的CuSO4的量比后者小,且与Cu反应时浓H2SO4变稀后不再反应,故C错误;
D.根据Cu与浓、稀HNO3反应的化学方程式可判断生成的NO2和NO的物质的量不相同,故D正确;
故选D.
B.由于Cu+Cl2=CuCl2,而2Cu+S=Cu2S,显然相同质量的铜参加反应,失去的电子数不相同,故B错误;
C.根据Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,CuO+H2SO4=CuSO4+H2O可知,相同物质的量的H2SO4(浓)参加反应,前者生成的CuSO4的量比后者小,且与Cu反应时浓H2SO4变稀后不再反应,故C错误;
D.根据Cu与浓、稀HNO3反应的化学方程式可判断生成的NO2和NO的物质的量不相同,故D正确;
故选D.
点评:本题考查铜单质的性质,铜与足量的稀硝酸、浓硝酸完全反应,生成气体的物质的量不同.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案
相关题目
下列有关实验原理或操作正确的是( )
A、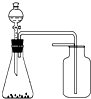 选择合适的试剂,装置可分别制取少量CO2、NO和O2 |
B、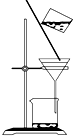 洗涤沉淀时(如图),向漏斗中加适量水,搅拌并滤干 |
| C、制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸 |
| D、用广泛pH试纸测得0.10 mol?L-1 NH4Cl溶液的pH=5.2 |
下列关于实验原理、操作的叙述,不正确的是( )
| A、除去乙酸乙酯中的乙酸,可以用饱和的碳酸钠溶液 |
| B、配制溶液时,俯视刻度线来定容,会使得所配溶液浓度偏高 |
| C、用托盘天平称取8.7克食盐 |
| D、实验室可以用新制氢氧化铜悬浊液来检验甘油,观察到的现象是出现绛蓝色沉淀 |
已知:乙醇可被强氧化剂氧化为乙酸. 可经三步反应制取
可经三步反应制取  ,发生反应的类型依次是( )
,发生反应的类型依次是( )
 可经三步反应制取
可经三步反应制取  ,发生反应的类型依次是( )
,发生反应的类型依次是( )| A、水解反应、加成反应、氧化反应 |
| B、加成反应、水解反应、氧化反应 |
| C、水解反应、氧化反应、加成反应 |
| D、加成反应、氧化反应、水解反应 |
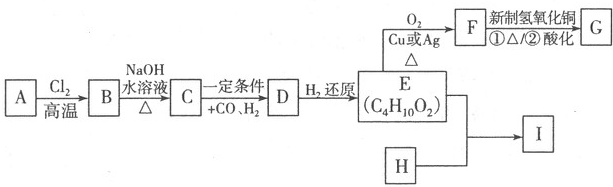
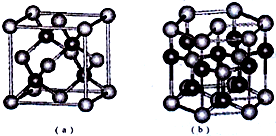 已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满.请根据以上信息,回答下列问题:
已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满.请根据以上信息,回答下列问题: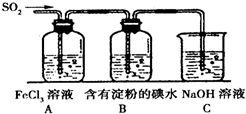 为探究SO2气体的还原性某兴趣小组设计了如装置图:
为探究SO2气体的还原性某兴趣小组设计了如装置图: