题目内容
16.下列事实与胶体性质无关的是( )| A. | 夏日的傍晚常常看到万丈霞光穿云而过美不胜收 | |
| B. | 受伤时,在流血的伤口上抹一点FeCl3可以止血 | |
| C. | “尿毒症”患者做血液透析治疗 | |
| D. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
分析 A.夏日的傍晚时看到的云属于胶体分散系,具有丁达尔现象;
B.胶体遇电解质发生聚沉;
C.血液是胶体,可用渗析提纯胶体;
D.三氯化铁溶液中滴入氢氧化钠溶液发生了复分解反应,与胶体性质无关.
解答 解:A.因云属于胶体分散系,则具有丁达尔现象,所以夏日的傍晚常常看到万丈霞光穿云而过美不胜收,与胶体有关,故A不选;
B.血液是胶体,胶体遇电解质发生聚沉,与胶体有关,故B不选;
C.尿毒症主要是血红蛋白随尿液排出,所以血液透析就是将血液通过半透膜,防止血红蛋白流失,故C不选;
D.三氯化铁与氢氧化钠反应生成氢氧化铁沉淀,两种溶液之间发生复分解反应,没有胶体,所以与胶体的性质无关,故D选;
故选D.
点评 本题考查胶体的性质,明确胶体常见的性质有丁达尔现象、胶体的聚沉、电泳等及其应用是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
6.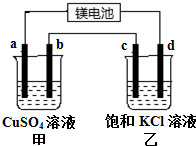 用一种镁二次电池(反应为:xMg+Mo3S4$?_{充电}^{放电}$MgxMo3S4)连接甲、乙装置进行电解.如图所示,a、b、c均为石墨电极,d为Fe电极,电解时d极有气体放出.下列说法不正确的是( )
用一种镁二次电池(反应为:xMg+Mo3S4$?_{充电}^{放电}$MgxMo3S4)连接甲、乙装置进行电解.如图所示,a、b、c均为石墨电极,d为Fe电极,电解时d极有气体放出.下列说法不正确的是( )
 用一种镁二次电池(反应为:xMg+Mo3S4$?_{充电}^{放电}$MgxMo3S4)连接甲、乙装置进行电解.如图所示,a、b、c均为石墨电极,d为Fe电极,电解时d极有气体放出.下列说法不正确的是( )
用一种镁二次电池(反应为:xMg+Mo3S4$?_{充电}^{放电}$MgxMo3S4)连接甲、乙装置进行电解.如图所示,a、b、c均为石墨电极,d为Fe电极,电解时d极有气体放出.下列说法不正确的是( )| A. | 甲装置中a的电极反应为4OH--4e-═O2↑+2H2O | |
| B. | 放电时镁电池正极的电极反应为 Mo3S4+2xe-═Mo3S42x- | |
| C. | 当d极产生0.56 L(标准状况)气体时,b极增重3.2 g | |
| D. | 镁电池放电时,甲池中的SO42-移向a电极 |
7.下列有关实验装置进行的相应实验,能达到实验目的是( )
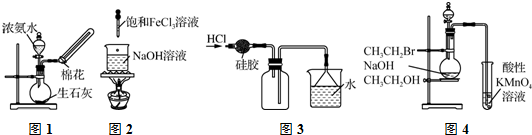

| A. | 利用图1所示装置制取少量NH3 | |
| B. | 利用图2所示装置制备Fe(OH)3胶体 | |
| C. | 利用图3所示装置收集HCl | |
| D. | 利用图4所示装置检验是否生成乙烯 |
11.有关晶胞的叙述正确的是( )
| A. | 晶胞是晶体结构中的基本结构单元 | |
| B. | 根据晶体的不同,晶胞可以是多种形状的几何体 | |
| C. | 晶胞一般都是平行六面体 | |
| D. | 晶胞都是正八面体 |
1.下列有关NaOH的说法正确的是( )
| A. | 属于共价化合物 | B. | 其中只含离子键 | ||
| C. | 氢氧根中含非极性键 | D. | 其中既含离子键,又含共价键 |
8.下列物质中,熵值(s)最大的是( )
| A. | 金刚石 | B. | Cl2(l) | C. | I2(g) | D. | Cu(s) |
12.已知室温时,0.1mol?L-1 某一元酸 HA 在水中有 0.1%发生电离,下列叙述错误的是( )
| A. | 该溶液的 pH=4 | |
| B. | 升高温度,溶液的 pH 增大 | |
| C. | 此酸的电离平衡常数约为 1×10-7 | |
| D. | 由 HA 电离出的 c(H+)约为水电离出的 c(H+)的106倍 |
13.不慎误服BaCl2后,可服用的解毒剂是( )
| A. | NaCl | B. | Na2CO3 | C. | AgNO3 | D. | MgSO4 |