题目内容
对于体积固定的密闭容器中进行的反应2SO2(气)+O2(气)?2SO3(气),下列判断正确的是( )
| A、容器内气体的密度保持不变 |
| B、当反应达到平衡状态时,SO3一定完全分解 |
| C、反应速率之比为v(SO2):v(O2):v(SO3)=2:1:2时,反应达到平衡 |
| D、反应达到平衡后,降低温度,平衡不发生移动 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:A.根据密度=
进行判断;
B.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物;
C.反应速率之比等于化学计量数之比;
D.降低温度,平衡向着放热的方向移动.
| 总质量 |
| 体积 |
B.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物;
C.反应速率之比等于化学计量数之比;
D.降低温度,平衡向着放热的方向移动.
解答:
解:A.密度=
,总质量不变,体积也不变,故容器内气体的密度保持不变,故A正确;
B.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故B错误;
C.反应速率之比等于化学计量数之比,故反应速率之比为v(SO2):v(O2):v(SO3)=2:1:2不能作为判断是否达到化学平衡状态的依据,故C错误;
D.正反应为放热反应,降低温度,平衡正向移动,故D错误,
故选A.
| 总质量 |
| 体积 |
B.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故B错误;
C.反应速率之比等于化学计量数之比,故反应速率之比为v(SO2):v(O2):v(SO3)=2:1:2不能作为判断是否达到化学平衡状态的依据,故C错误;
D.正反应为放热反应,降低温度,平衡正向移动,故D错误,
故选A.
点评:本题考查化学平衡状态的判断、可逆反应的特点、平衡移动原理等,难度不大.要注意把握平衡状态的特征.

练习册系列答案
相关题目
下列关于反应速率的说法中,错误的是( )
| A、反应速率可用于衡量化学反应的快慢 |
| B、决定反应速率的主要因素是温度和压强 |
| C、可逆反应达到化学平衡时,正、逆反应速率相等且不为零 |
| D、增大反应物浓度,提高反应物温度都能增大反应速率 |
下列事实不能用勒夏特列原理解释的是( )
| A、新制的氯水在光照条件下颜色变浅 |
| B、打开可乐瓶盖后看到有大量气泡逸出 |
| C、已知2HI(g)?H2(g)+I2(g),对容积可变的密闭容器中已达平衡的HI、I2、H2混合气体进行压缩,混合气体颜色变深 |
| D、工业上用氮气、氢气合成氨气的过程中,通过加压将氨气液化以增大转化率 |
乙烯雌酚是一种激素类药物,结构如图,下列有关叙述不正确的是( )
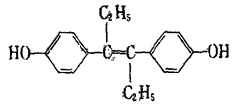

| A、它易溶于有机溶剂 |
| B、1mol该有机物最多消耗NaOH和Na2CO3的物质的量均为2mol |
| C、1mol该有机物可以与5mol Br2发生反应 |
| D、该有机物分子中,最多有14个碳原子共平面 |
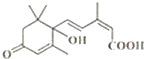 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、分子式为C15H22O4 |
| B、1mol该物质最多可以消耗H2和Br2的量分别为4mol和3mol |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、该物质可以发生分子内酯化反应形成六元环,也可以发生缩聚反应和加聚反应 |
下列物质在光照的条件下不会发生化学变化的是( )
| A、H2和Cl2的混合气体 |
| B、氯水 |
| C、AgBr |
| D、Na2CO3 |
等物质的量浓度的下列物质的溶液①NaCl ②CH3COONa ③NH4Cl ④Ba(OH)2 ⑤NaHSO4 ⑥Na2CO3 ⑦NaHCO3 ⑧H2SO4 ⑨NaOH,其pH值由大到小的顺序是( )
| A、④⑨⑥⑦②①③⑤⑧ |
| B、⑧⑤③①⑦②⑥⑨④ |
| C、④⑨⑥②⑦①⑤③⑧ |
| D、④⑨⑥②⑦①③⑤⑧ |
下列物质分离或提纯的方法,属于化学方法的是( )
| A、蒸馏使沸点低液体蒸出 |
| B、过滤除去不溶性杂质 |
| C、加热使杂质分解成气体 |
| D、萃取分液使溶质转移到另一溶剂中 |