题目内容
18. 数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果.
数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果.已知:C(s)+O2(g)═CO2(g);△H=-393kJ•mol-1
2CO (g)+O2(g)═2CO2(g);△H=-566kJ•mol-1
2H2(g)+O2(g)═2H2O(g);△H=-484kJ•mol-1
(1)工业上常采用将水蒸气喷到灼热的炭层上实现煤的气化(制得CO、H2),该反应的热化学方程式是C(s)+H2O(g)=CO(g)+H2(g)△H=+132kJ•mol-1
(2)上述煤气化过程中需向炭层交替喷入空气和水蒸气,喷入空气的目的是让部分炭燃烧,提供炭与水蒸气反应所需要的热量;该气化气可在适当温度和催化剂下合成液体燃料甲醇,该反应方程式为CO+2H2$\frac{\underline{\;一定温度\;}}{催化剂}$CH3OH
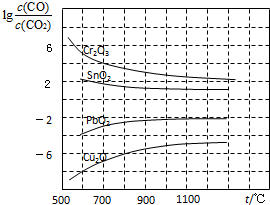
(3)CO常用于工业冶炼金属,如图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图.
下列说法正确的是BC
A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D.CO还原PbO2的反应△H>0
(4)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2$\frac{\underline{\;电解\;}}{\;}$2CO+O2,则其阳极的电极反应式为4OH--4e-=O2↑+2H2O.
(5)将CO通入银氨溶液中可析出黑色的金属颗粒,写出反应方程式CO+2Ag(NH3)2OH=2Ag↓+(NH4)2CO3+2NH3.
分析 (1)水蒸气喷到灼热的炭层上实现煤的气化(制得CO、H2)即反应方程式为C(s)+H2O(g)=CO (g)+H2(g),再根据盖斯定律进行计算;
(2)根据(1)煤和水蒸气的反应生成一氧化碳和氢气要吸热,故喷入空气的目的是让部分炭燃烧,提供炭与水蒸气反应所需要的热量;一氧化碳和氢气,在一定条件下合成甲醇,据此书写方程式;
(3)A、增高炉的高度,增大CO与铁矿石的接触,不能影响平衡移动,CO的利用率不变;
B、由图象可知用CO工业冶炼金属铬时,lg[c(CO)/c(CO2)]一直很高,说明CO转化率很低,故不适合;
C、由图象可知温度越低lg[c(CO)/c(CO2)]越小,故CO转化率越高;
D、由图象可知CO还原PbO2的温度越高lg[c(CO)/c(CO2)]越高,说明CO转化率越低,平衡逆向移动,故△H<0;
(4)依据电解原理阴极上是得到电子发生还原反应生成一氧化碳;
(5)CO与银氨溶液反应将银氨溶液还原成黑色的银,本身在碱性溶液中被氧化成碳酸根.
解答 解:(1)已知:①C(s)+O2(g)=CO2(g);△H=-393kJ•mol-1
②2CO (g)+O2(g)=2CO2(g);△H=-566kJ•mol-1
③2H2(g)+O2(g)=2H2O(g);△H=-484kJ•mol-1
将(①×2-②-③)×$\frac{1}{2}$得到反应C(s)+H2O(g)=CO (g)+H2(g),则△H═(-393kJ•mol-1×2+566kJ•mol-1+484kJ•mol-1)×$\frac{1}{2}$=+132 kJ•mol-1
故答案为:C(s)+H2O(g)=CO (g)+H2(g)△H=+132 kJ•mol-1;
(2)根据(1)煤和水蒸气的反应生成一氧化碳和氢气要吸热,故喷入空气的目的是让部分炭燃烧,提供炭与水蒸气反应所需要的热量;
一氧化碳和氢气在一定条件下合成甲醇的原理为:CO+2H2$\frac{\underline{\;一定温度\;}}{催化剂}$CH3OH;
故答案为:让部分炭燃烧,提供炭与水蒸气反应所需要的热量;CO+2H2$\frac{\underline{\;一定温度\;}}{催化剂}$CH3OH;
(3)A、增高炉的高度,增大CO与铁矿石的接触,不能影响平衡移动,CO的利用率不变,故A错误;
B、由图象可知用CO工业冶炼金属铬时,lg[c(CO)/c(CO2)]一直很高,说明CO转化率很低,故不适合B正确;
C、由图象可知温度越低lg[c(CO)/c(CO2)]越小,故CO转化率越高,故C正确;
D、由图象可知CO还原PbO2的温度越高lg[c(CO)/c(CO2)]越高,说明CO转化率越低,平衡逆向移动,故△H<0,故D错误;
故选:BC;
(4)以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2$\frac{\underline{\;电解\;}}{\;}$2CO+O2,则溶液中的氢氧根在阳极上失去电子发生氧化反应生成氧气,电极反应式为:4OH--4e-=O2↑+2H2O;
故答案为:4OH--4e-=O2↑+2H2O;
(5)CO与银氨溶液反应将银氨溶液还原成黑色的银,本身在碱性溶液中被氧化成碳酸根,故反应的化学方程式为CO+2Ag(NH3)2OH=2Ag↓+(NH4)2CO3+2NH3
故答案为:CO+2Ag(NH3)2OH=2Ag↓+(NH4)2CO3+2NH3.
点评 本题主要考查了盖斯定律的应用、电极方程式及其化学方程式的书写、根据图象对平衡移动的判断等,重在培养学生能够利用化学知识提取题干的信息进行答题的能力,综合性强,难度较大;

 阅读快车系列答案
阅读快车系列答案①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
| A. | 一定含有Fe3+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Fe3+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c (Al3+)=1.00 mol•L-1 | |
| D. | c(Na+)=0.50 mol•L-1 |
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定呈碱性 | |
| C. | 某无色溶液中加入BaCl2溶液,再加稀盐酸,沉淀不溶解,原溶液中一定有SO42- | |
| D. | 某无色溶液中加入酚酞试液变红,该溶液一定是碱溶液 |
| A. | 碱性氧化物均为金属氧化物 | |
| B. | 一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物 | |
| C. | 酸根离子中不可能含有金属元素 | |
| D. | 还原产物只有还原性,氧化产物只有氧化性 |
| A. | 少量NaHCO3与过量Ca(OH)2反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 在CuSO4溶液中加Ba(OH)2溶液 SO42-+Ba2+═BaSO4↓ | |
| C. | Na2S溶液中通入H2S气体 S2-+H+═HS- | |
| D. | NaHCO3溶液与KHSO4溶液反应 HCO3-+H+═CO2↑+H2O |
 乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:①部分物质的沸点:
| 物质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
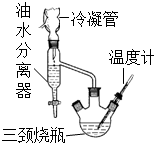
③水、乙醇、苯的混合物在64.85℃时,能按一定的比例以共沸物的形式一起蒸发.该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
第一步:在三颈烧瓶中加入0.1mol无水乳酸、过量的65.0mL无水乙醇、一定量的苯、沸石…;装上油水分离器和冷凝管,缓慢加热回流至反应完全.
第二步:将三颈烧瓶中液体倒入盛有过量某试剂的烧杯中,搅拌并分出有机相后,再用水洗.
第三步:将无水CaCl2加入到水洗后的产品中,过滤、蒸馏.
(1)第一步操作中,还缺少的试剂是浓硫酸;加入苯的目的是形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行;实验过程中,酯化反应进行完全的标志是油水分离器中液体不再增加.
(2)第二步中证明“水洗”已经完成的实验方案是测定水洗液的pH至7.
(3)利用核磁共振氢谱可以鉴定制备的产物是否为乳酸乙酯,乳酸乙酯分子核磁共振氢谱中有5个峰.

