题目内容
17.下列有关化学用语的理解错误的是( )| A. |  表示丙烯的键线式 表示丙烯的键线式 | B. |  表示甲烷分子球棍模型 表示甲烷分子球棍模型 | ||
| C. | C2H4O2表示乙酸的分子式 | D. |  34S2-的结构示意图 34S2-的结构示意图 |
分析 A.键线式就是只用键线来表示碳架,而分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略,而其他杂原子及与杂原子相连的氢原子须保留;
B.该模型是比例模型;
C.乙酸是含一个羧基的饱和羧酸,结构简式为CH3COOH;
D.34S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,用小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数;
解答 解:A.丙烯的键线式 ,故A正确;
,故A正确;
B.甲烷分子的球棍模型为 ,故B错误;
,故B错误;
C.乙酸是含一个羧基的饱和羧酸,结构简式为CH3COOH,分子式为:C2H4O2,故C正确;
D.34S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,硫离子结构示意图为 ,故D正确;
,故D正确;
故选B.
点评 本题考查了常见的化学用语,该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、原子结构、原子结构示意图、结构式、结构简式以及各种模型等,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
7.在100ml 混合酸中,HNO3和H2SO4的物质的量浓度分别为0.4mol/L 和0.1mol/L,向该混合液中加1.92g 铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度是( )
| A. | 0.15 mol/L | B. | 0.225 mol/L | C. | 0.35 mol/L | D. | 0.45 mol/L |
5.下列化学方程式中,不属于水解反应的是( )
| A. | CH≡CH+H2O $→_{△}^{HgSO_{4}}$CH3CHO | |
| B. | C2H5Br+H2O $→_{△}^{NaOH}$ C2H5OH+HBr | |
| C. | CaC2+2H2O→Ca(OH)2+C2H2↑ | |
| D. | CH3COOCH3+H2O$→_{△}^{催化剂}$CH3COOH+CH3OH |
5.碱性锌锰电池是一种高效的一次电池,外壳为金属锌,中间是石墨极,以MnO2为正极反应物KOH溶液作为电解质溶液,现由碱性锌锰电池回收一些物质.已知Zn2+和Mn2+沉淀的ph范围如下表所示:
请回答下列问题:
(1)该电池的正极反应为MnO2+e-+H+═MnOOH,总反应为Zn+2MnO2+2H+═Zn2++2MnOOH.
(2)该电池中转移0.2mol电子时,消耗MnO2的质量为17.4g.
(3)将该电池的负极材料和MnO2与足量的浓盐酸共热,其中MnO2参与反应的离子方程式为MnO2+4H+(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;欲使Mn2+和Zn2+分离,需调整pH为6.2≤pH<8.2,可以加入Mn(OH)2调节pH.
(4)再继续调大pH可得到Mn(OH)2,该沉淀在空气中可以迅速被氧化成MnO2,写出此反应的化学方程式2Mn(OH)2+O2=2MnO2+2H2O.
(5)根据Mn2+沉淀完全的pH可以求得Mn(OH)2的Ksp约为10-24.4.
| 离子 | 开始沉淀 | 沉淀完全 |
| Zn2+ | 5.7 | 6.2 |
| Mn2+ | 8.2 | 9.7 |
(1)该电池的正极反应为MnO2+e-+H+═MnOOH,总反应为Zn+2MnO2+2H+═Zn2++2MnOOH.
(2)该电池中转移0.2mol电子时,消耗MnO2的质量为17.4g.
(3)将该电池的负极材料和MnO2与足量的浓盐酸共热,其中MnO2参与反应的离子方程式为MnO2+4H+(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;欲使Mn2+和Zn2+分离,需调整pH为6.2≤pH<8.2,可以加入Mn(OH)2调节pH.
(4)再继续调大pH可得到Mn(OH)2,该沉淀在空气中可以迅速被氧化成MnO2,写出此反应的化学方程式2Mn(OH)2+O2=2MnO2+2H2O.
(5)根据Mn2+沉淀完全的pH可以求得Mn(OH)2的Ksp约为10-24.4.
12.下列关于电池的说法正确的是( )
| A. | 电解含CuSO4和NaCl的溶液,在阴极可能析出气体,阳极一定析出气体 | |
| B. | 电解CuCl2溶液可得到铜和氯气,阴极区酸性减弱,阳极区pH不变 | |
| C. | 碱性锌锰干电池的负极反应为:Zn-2e-+4OH-═ZnO22-+2H2O | |
| D. | 原电池负极金属一定比正极金属的金属性活泼 |
9.化学能与热能、电能等能相互转化,关于化学能与其他能量相互转化的说法错误的是( )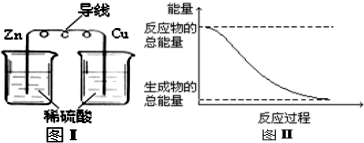

| A. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| B. | 化石燃料是可再生性能源,燃烧时将化学能转变为热能 | |
| C. | 图I所示的装置不能将化学能转变为电能 | |
| D. | 图II所示的反应为放热反应 |
10.下列叙述不正确的是( )
| A. | 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火 | |
| B. | 纳米铁粉可以高效地去除被污染水体的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附 | |
| C. | 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线 | |
| D. | Ba2+浓度较高时危害健康,但BaSO4可服入体内,做为造影剂用于X-射线检查肠胃道疾病 |