题目内容
9.化学能与热能、电能等能相互转化,关于化学能与其他能量相互转化的说法错误的是( )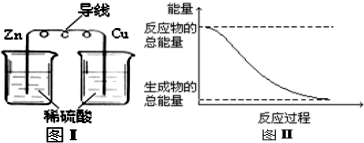
| A. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| B. | 化石燃料是可再生性能源,燃烧时将化学能转变为热能 | |
| C. | 图I所示的装置不能将化学能转变为电能 | |
| D. | 图II所示的反应为放热反应 |
分析 A.化学反应时断键要吸收能量,成键要放出能量;
B.化石燃料是不可再生能源;
C.图I所示的装置没形成闭合回路,不能形成原电池;
D.图II所示的反应,反应物的总能量大于生成物的总能量.
解答 解:A.化学反应时断键要吸收能量,成键要放出能量,所以化学反应中能量变化的主要原因是化学键的断裂与生成,故A正确;
B.化石燃料是不可再生能源,在地球上蕴藏量是有限的,故B错误;
C.图I所示的装置没形成闭合回路,不能形成原电池,没有电流通过,所以不能把化学能转变为电能,故C正确;
D.图II所示的反应,反应物的总能量大于生成物的总能量,所以该反应为放热反应,故D正确;
故选B.
点评 本题主要是考查学生对化学反应中能量变化对的原因、影响反应热大小因素以及原电池构成条件的熟悉了解程度,旨在培养学生灵活运用基础知识解决实际问题的能力,注意相关知识的积累和总结,题目难度中等.

练习册系列答案
相关题目
16.如图是氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )
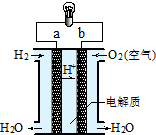

| A. | b极是正极 | |
| B. | 负极的电极反应式为:O2+2H2O+4e-=4OH- | |
| C. | 电子由a通过灯泡流向b | |
| D. | 氢氧燃料电池是环保电池 |
17.下列有关化学用语的理解错误的是( )
| A. |  表示丙烯的键线式 表示丙烯的键线式 | B. |  表示甲烷分子球棍模型 表示甲烷分子球棍模型 | ||
| C. | C2H4O2表示乙酸的分子式 | D. |  34S2-的结构示意图 34S2-的结构示意图 |
4.某烃在氧气中完全燃烧,生成等物质的量的CO2和H2O,该烃在气态时的密度是相同条件下氢气的35倍.试求:
(1)该有机化合物的分子式.
(2)若分子中只有两个甲基且属于不饱和烃,写出其可能的结构简式.
(1)该有机化合物的分子式.
(2)若分子中只有两个甲基且属于不饱和烃,写出其可能的结构简式.
14.下列表示对应化学反应离子方程式正确的是( )
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | FeCl3溶液于Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| D. | 过量氯气通入FeI2溶液中:3Cl2+2I-+4Fe2+═I2+4Fe3++4Cl- |
1.下列叙述不正确的是( )
①热稳定性:H2O>HF>H2S ②熔点:Al>Na>K
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素⑤沸点:NH3<PH3<AsH3
⑥因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
①热稳定性:H2O>HF>H2S ②熔点:Al>Na>K
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素⑤沸点:NH3<PH3<AsH3
⑥因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N.
| A. | ②④⑥ | B. | ①③⑤⑥ | C. | ②④⑥ | D. | ①③④⑤⑥ |
18.下列物质中,中心原子的杂化方式不是sp3杂化的是( )
| A. | SO2 | B. | CH4 | C. | NH3 | D. | SO42- |
