题目内容
12.将等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,再滴入含有品红和BaCl2的混合溶液,则发生的实验现象是( )①红色溶液很快褪色 ②红色溶液不褪色 ③有白色沉淀生成 ④溶液仍然透明.
| A. | 仅①和④ | B. | 仅①和③ | C. | 仅②和③ | D. | 仅②和④ |
分析 将等物质的量的SO2和Cl2反应生成盐酸和硫酸,依据盐酸和硫酸的性质判断发生反应及现象,据此解答.
解答 解:等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,发生:SO2+Cl2+2H2O=2HCl+H2SO4,
生成盐酸和硫酸都不具有漂白性,所以不能使品红溶液褪色,硫酸与氯化钡反应生成硫酸钡沉淀,所以会产生白色沉淀,
故选:C.
点评 本题考查氯气和二氧化硫的反应,明确二者发生反应及生成物的性质是解题关键,题目难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
3.下列说法中正确的是( )
| A. | 物质发生化学反应时不一定都伴随着能量变化 | |
| B. | 伴有能量变化的变化都是化学变化 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 |
 .
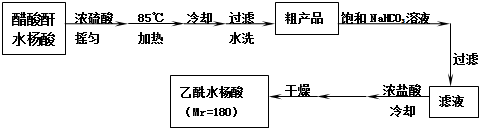
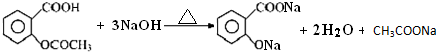
. 阿司匹林口服时,具有解热镇痛作用,是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄.近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成;它的有效成分是乙酰水杨酸(
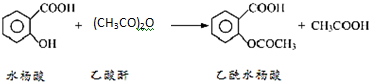
阿司匹林口服时,具有解热镇痛作用,是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄.近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成;它的有效成分是乙酰水杨酸(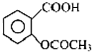 ).
).
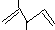 名称:2,3-二甲基-1,5-戊二烯 ②乙烯的实验式;CH2
名称:2,3-二甲基-1,5-戊二烯 ②乙烯的实验式;CH2