题目内容
20.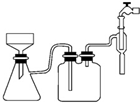 阿司匹林口服时,具有解热镇痛作用,是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄.近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成;它的有效成分是乙酰水杨酸(
阿司匹林口服时,具有解热镇痛作用,是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄.近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成;它的有效成分是乙酰水杨酸(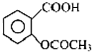 ).
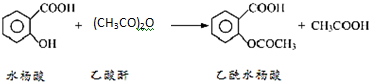
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸.
【反应原理及部分装置】
【实验流程】
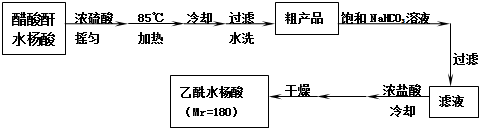
已知:①醋酸酐遇水分解生成醋酸.
②水杨酸和乙酰水杨酸均微溶于水,但其钠盐易溶于水,副产物为高分子化合物,难溶于水.
回答下列问题:
(1)合成过程中要控制温度在85℃~90℃,最合适的加热方法水浴加热.
(2)用图装置过滤比普通漏斗过滤的优点是过滤速度快、得到的产品较干燥.
(3)粗产品提纯:
①分批用少量饱和NaHCO3溶液溶解粗产品,目的是使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,便于与杂质分离;判断该过程结束的现象是没有气体(CO2)产生.
②加浓盐酸、冷却后的操作是过滤、洗涤、干燥、称重、计算产率.
③纯度检验:取少许产品加入盛有2mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色,可能的原因是产品中仍然可能含有水杨酸.
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):
Ⅰ.称取阿司匹林样品m g;
Ⅱ.将样品研碎,溶于V1 mL a mol/LNaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;
Ⅲ.向锥形瓶中滴加几滴甲基橙,用浓度为b mol/L的标准盐酸滴定剩余的NaOH,消耗盐酸的体积为V2mL.
已知 乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式:
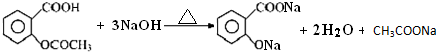
则阿司匹林药片中乙酰水杨酸质量分数的表达式为:$\frac{0.180(a{V}_{1}-b{V}_{2})}{3m}$.
分析 醋酸酐和水杨酸混合,然后向混合溶液中加入浓硫酸,相当于浓硫酸的稀释,并不断搅拌,防止局部受热而产生安全事故;摇匀后加热至85℃,然后冷却、过滤、水洗得到粗产品,然后向粗产品中加入饱和碳酸氢钠溶液,使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,从而除去杂质;然后用浓盐酸洗涤剩余的碳酸氢钠、将乙酰水杨酸钠转化为乙酰水杨酸,最后过滤、洗涤、干燥得到乙酰水杨酸;
(1)温度低于100℃时采用水浴加热;
(2)用图装置过滤比普通漏斗过滤,其优点是过滤速度快、得到的产品较干燥;
(3)①使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,乙酰水杨酸钠易溶于水;
②加浓盐酸、冷却后的操作是过滤、洗涤;
③酚羟基能和氯化铁发生显色反应;
(4)根据题意计算乙酰水杨酸消耗的氢氧化钠的物质的量,结合乙酰水杨酸的物质的量是消耗的氢氧化钠的物质的量的$\frac{1}{3}$,可以得到阿司匹林药片中乙酰水杨酸质量分数.
解答 解:醋酸酐和水杨酸混合,然后向混合溶液中加入浓硫酸,相当于浓硫酸的稀释,并不断搅拌,防止局部受热而产生安全事故;摇匀后加热至85℃,然后冷却、过滤、水洗得到粗产品,然后向粗产品中加入饱和碳酸氢钠溶液,使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,从而除去杂质;然后用浓盐酸洗涤剩余的碳酸氢钠、将乙酰水杨酸钠转化为乙酰水杨酸,最后过滤、洗涤、干燥得到乙酰水杨酸;
(1)温度低于100℃时采用水浴加热,该操作中温度小于100℃,所以需要水浴加热,
故答案为:水浴加热;
(2)用图装置过滤比普通漏斗过滤,其优点是过滤速度快、得到的产品较干燥,
故答案为:过滤速度快、得到的产品较干燥;
(3)①使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,乙酰水杨酸钠易溶于水,从而除去杂质,且便于分离;乙酰水杨酸能和碳酸氢钠反应生成二氧化碳气体,所以判断该过程结束的现象是没有气体(CO2)产生;
故答案为:使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,便于与杂质分离;没有气体(CO2)产生;
②加浓盐酸、冷却后的操作是过滤、洗涤、干燥,从而得到较纯净、干燥的物质,
故答案为:过滤;洗涤;
③酚羟基能和氯化铁发生显色反应,加入氯化铁溶液后混合溶液呈紫色,说明产品中仍然可能含有水杨酸,
故答案为:产品中仍然可能含有水杨酸;
(4)乙酰水杨酸消耗的氢氧化钠的物质的量为:aV1×10-3-bV2×10-3,乙酰水杨酸的物质的量是消耗的氢氧化钠的物质的量的$\frac{1}{3}$,阿司匹林药片中乙酰水杨酸质量分数的表达式为$\frac{0.180(a{V}_{1}-b{V}_{2})}{3m}$,故答案为:$\frac{0.180(a{V}_{1}-b{V}_{2})}{3m}$.
点评 本题考查物质制备,为高频考点,明确实验原理、实验操作方法、实验先后顺序是解本题关键,知道每一步可能发生的反应、基本操作方法,知道物质分离提纯方法与物质性质关系,题目难度不大.

仪器装置:
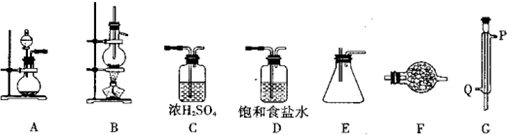
已知四氯化锡具有强的吸水性,水解生成锡的氧化物.SnCl4和Sn的部分数据如下:
| 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | |
| 四氯化锡 | 2.2 | -33 | 114 |
| 金属锡 | 5.77 | 231 |
(1)实验时装置的正确连接顺序为AD→C→B→G→E→F
(2)仪器G的名称是冷凝管实验时,冷却水的流向是从Q进入(填符号)
(3)A中反应的离子方程式2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(4)F中盛装的化学试剂是碱石灰;;作用是防止空气中的水分进入装置E中、吸收多余的Cl2防止污染.写出SnCl4水解的化学方程式SnCl4+4H2O=Sn(OH)4+4HCl
(5)实验完毕后,E装置质量增加9.4g,SnCl4的产率是90%.
| A. | 间二甲苯的二氯代物有5种 | |
| B. | 二氯甲烷有2种同分异构体 | |
| C. | 丙烯分子中所有的原子有可能在同一平面上 | |
| D. | 用-C4H9取代苯环上的1个氢原子,最多可得4种同分异构体 |
| A. | ①④②⑤③ | B. | ⑤②①④③ | C. | ②⑤④①③ | D. | ④①②⑤③ |

| A. | 甲:NaOH; 乙:稀盐酸 | B. | 甲:水; 乙:氢氧化钠溶液 | ||
| C. | 甲:氢氧化钠溶液; 乙:水 | D. | 甲:稀盐酸; 乙:氯化钠溶液 |
| A. | 淀粉胶体加入电解质可发生聚沉现象 | |
| B. | 向Fe(OH)3胶体中加入少量H2SO4溶液,会生成红褐色沉淀 | |
| C. | 可利用丁达尔效应区分胶体与溶液 | |
| D. | 胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 |
①红色溶液很快褪色 ②红色溶液不褪色 ③有白色沉淀生成 ④溶液仍然透明.
| A. | 仅①和④ | B. | 仅①和③ | C. | 仅②和③ | D. | 仅②和④ |
| 编号 | Ⅰ | Ⅱ |
| 实验一 | 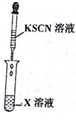  | 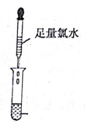 |
| 编号 | Ⅲ | |
| 实验二 |  | |
(2)实验步骤Ⅲ中反应的离子方程式为:Cl-+Ag+=AgCl↓;
(3)实验一证明X溶液中含Fe2+离子,实验Ⅱ证明X溶液中含Cl-离子.(填离子符号)
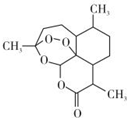 北京时问2015年10月5日,中国女科学家屠哟哟获颁诺贝尔医学奖.屠哟哟从中医古籍里得到启发,用乙醚从青蒿中提取出可以高效抑制疟原虫的成分-青蒿素(结构简式如图),这一发现在全球范围内挽救了数以百万人的生命.下列说法中不正确的是( )
北京时问2015年10月5日,中国女科学家屠哟哟获颁诺贝尔医学奖.屠哟哟从中医古籍里得到启发,用乙醚从青蒿中提取出可以高效抑制疟原虫的成分-青蒿素(结构简式如图),这一发现在全球范围内挽救了数以百万人的生命.下列说法中不正确的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素能与NaOH溶液反应 | |
| C. | 青蒿素易溶于水、乙醇、苯等溶剂 | |
| D. | 用乙醚从青蒿中提取青蒿素,用到了萃取的原理 |