题目内容
2.请按指定要求完成下列问题.(1)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被水所还原的BrF3的物质的量是$\frac{4}{3}$mol
(2)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目
 .
.②若生成0.2mol AsH3,则转移的电子数为1.2NA.
(3)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4═2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为1:1;
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两方法中消耗的还原剂质量之比为73:34.
分析 (1)3BrF3+5H2O═HBrO3+Br2+9HF+O2中,Br元素的化合价分别由+3价升高为+5价、由+3价降低为0,O元素的化合价由-2价升高为0;
(2)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中Zn元素的化合价升高,As元素的化合价降低,该反应转移电子为12e-;
(3)①2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O中,NaClO3为氧化剂,HCl为还原剂,只有一半HCl作还原剂;
②得到相同条件下相同体积的ClO2气体,设均生成2mol,方法一中作还原剂的HCl为2mol,方法二中作还原剂的H2O2为1mol;
解答 解:(1)当有5mol水参加反应时,O元素化合价由-2价升高到0价,2mol水被氧化,失去4mol电子,Br元素化合价由+3价降低到0价,则由H2O还原的BrF3为$\frac{4mol}{3-0}$=$\frac{4}{3}$mol,
故答案为:$\frac{4}{3}$mol;
(2)①As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中Zn元素的化合价升高,As元素的化合价降低,该反应转移电子为12e-,用双线桥法标出电子转移的方向和数目为 ,
,
故答案为: ;
;
②若生成0.2mol AsH3,由As元素的化合价由+3价降低为-3价可知转移的电子数为0.2mol×6×NA=1.2NA,
故答案为:1.2NA;
(3)①2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O中,NaClO3为氧化剂,HCl为还原剂,只有一半HCl作还原剂,由反应可知氧化剂与还原剂的物质的量之比为2mol:2mol=1:1,
故答案为:1:1;
②得到相同条件下相同体积的ClO2气体,设均生成2mol,方法一中作还原剂的HCl为2mol,方法二中作还原剂的H2O2为1mol,可知两方法中消耗的还原剂质量之比为2mol×36.5g/mol:1mol×34g/mol=73:34,
故答案为:73:34.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应及电子转移计算、物质的量的有关计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 合成氨工业中,氢气的转化率 | B. | 醋酸钠的水解程度 | ||
| C. | 水的离子积 | D. | 氢气的溶解度 |
仪器装置:
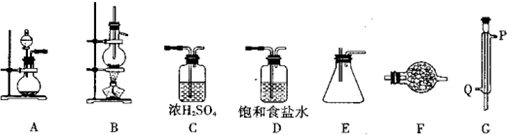
已知四氯化锡具有强的吸水性,水解生成锡的氧化物.SnCl4和Sn的部分数据如下:
| 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | |
| 四氯化锡 | 2.2 | -33 | 114 |
| 金属锡 | 5.77 | 231 |
(1)实验时装置的正确连接顺序为AD→C→B→G→E→F
(2)仪器G的名称是冷凝管实验时,冷却水的流向是从Q进入(填符号)
(3)A中反应的离子方程式2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(4)F中盛装的化学试剂是碱石灰;;作用是防止空气中的水分进入装置E中、吸收多余的Cl2防止污染.写出SnCl4水解的化学方程式SnCl4+4H2O=Sn(OH)4+4HCl
(5)实验完毕后,E装置质量增加9.4g,SnCl4的产率是90%.
| A. | 强电解质在水溶液中的电离过程是不可逆的 | |
| B. | 强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强 | |
| C. | 易溶于水的电解质一定是强电解质 | |
| D. | 同一弱电解质溶液,温度不同时,导电能力相同 |
| A. | 间二甲苯的二氯代物有5种 | |
| B. | 二氯甲烷有2种同分异构体 | |
| C. | 丙烯分子中所有的原子有可能在同一平面上 | |
| D. | 用-C4H9取代苯环上的1个氢原子,最多可得4种同分异构体 |
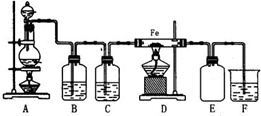 实验室可以用浓盐酸与二氧化锰在加热的条件下反应生成二氯化锰与氯气,纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如图,回答下列问题:
实验室可以用浓盐酸与二氧化锰在加热的条件下反应生成二氯化锰与氯气,纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如图,回答下列问题: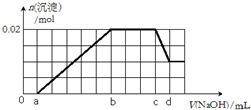 有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验: [Al(OH)2]++H+.
[Al(OH)2]++H+.