题目内容
1.下列各组物质中,化学键完全相同的是( )| A. | NaCl和NaOH | B. | Cl2和N2O | C. | Na2S和(NH4)2S | D. | H2O2和Na2O2 |
分析 A、NaCl中只有离子键,而NaOH中存在离子键和共价键;
B、Cl2中只存在共价键的单质,而N2O中也只存共价键的化合物;
C、Na2S中只存在离子键;(NH4)2S中存在离子键和共价键;
D、H2O2中只存在共价键,Na2O2中存在离子键和非极性共价键.
解答 解:A、NaCl中只有离子键,而NaOH中存在离子键和共价键,所以两者化学键不完全相同,故A错误;
B、Cl2中只存在共价键的单质,而N2O中也只存共价键的化合物,两者化学键完全相同,故B正确;
C、Na2S中只存在离子键;(NH4)2S中存在离子键和共价键,所以两者化学键不完全相同,故C错误;
D、H2O2中只存在共价键,Na2O2中存在离子键和非极性共价键,所以两者化学键不完全相同,故D错误;
故选B.
点评 本题考查了化学键的判断,根据物质的构成微粒及微粒间的作用力来分析解答,知道离子键、共价键的区别,题目难度不大.

练习册系列答案
相关题目
12. 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )| A. | 6:1 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
16.依据下列甲、乙、丙三图,判断下列叙述不正确的是( )
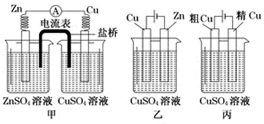

| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙、丙装置中,阳极均发生氧化反应而溶解 | |
| D. | 丙装置中,铜电极的质量有增有减 |
6.如图是元素周期表的轮廓图,通常用于制造农药的元素所在的区域是( )
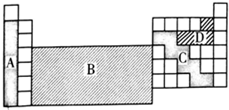

| A. | A | B. | B | C. | C | D. | D |
13.在一定条件下MO3-与M-发生反应;MO3-+5M-+6H+═3M2+3H2O,则下列关于M元素的叙述中正确的是( )
| A. | M的氢化物的水溶液呈酸性 | B. | M2在常温常压下一定是气体 | ||
| C. | MO3-中的M元素只能被还原 | D. | M位于元素周期表的第VA族 |
10.地壳中含量居第一位的金属元素是( )
| A. | 铁 | B. | 铝 | C. | 氧 | D. | 硅 |
 .
.
 .
. .
.