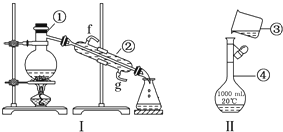
题目内容
16.依据下列甲、乙、丙三图,判断下列叙述不正确的是( )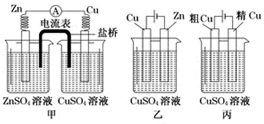
| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙、丙装置中,阳极均发生氧化反应而溶解 | |
| D. | 丙装置中,铜电极的质量有增有减 |
分析 A、甲装置没有外加电源,属于原电池,乙装置存在外加电源,属于电解池;
B、在原电池的负极上发生氧化反应,在电解池的阴极上,发生还原反应;
C、在电解池的阳极上发生的是失电子的氧化反应,根据电极材料确定发生的反应;
D、丙装置中,粗铜电极发生氧化反应,质量减少;精铜上电解质溶液中的铜离子放电生成单质铜,质量增加.
解答 解:A、甲装置没有外加电源,属于原电池,乙装置存在外加电源,属于电解池,可以在锌上镀铜,故A正确;
B、甲装置中,锌是负极,该电极上锌失电子发生氧化反应,乙装置中,锌极是阴极,该电极上发生还原反应,故B错误;
C、乙、丙装置中,阳极均是活泼的金属电极,该电极发生氧化反应而溶解,故C正确;
D、丙装置中,粗铜电极发生氧化反应,质量减少;精铜上电解质溶液中的铜离子放电生成单质铜,质量增加,所以铜电极的质量有增有减,故D正确.
故选B.
点评 本题考查学生原电池和电解池的工作原理知识,注电镀池的特点以及电解精炼铜装置的特点区别是关键,难度中等.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
4.同温同压下,体积相同的两个容器,一个充满NO,另外一个充满N2 和O2的混合气体,这两个容器中一定相同的是( )
| A. | 原子总数 | B. | 质子总数 | C. | 电子总数 | D. | 质量 |
11.关于如图所示装置的叙述,正确的是( )


| A. | 此装置为原电池,铜片上有气泡产生 | |
| B. | 铜片质量逐渐减少 | |
| C. | 电流从锌片经导线流向铜片 | |
| D. | 氢离子在铜片表面被氧化 |
1.下列各组物质中,化学键完全相同的是( )
| A. | NaCl和NaOH | B. | Cl2和N2O | C. | Na2S和(NH4)2S | D. | H2O2和Na2O2 |
8. 过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
 过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )| A. | 过氧化氢分子中含有H-H键、O-O键 | |
| B. | 过氧化氢分子中存在离子键和共价键 | |
| C. | 过氧化氢分子中只有共价键,其电子式为 | |
| D. | H2O2与H2O互为同位素 |
5.下列化学用语正确的是( )
| A. | 氟化氢的电子式: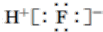 | B. | 中子数为21的钾原子:${\;}_{19}^{40}$K | ||
| C. | NH3的结构式: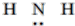 | D. | N3-的结构示意图: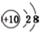 |
 ;
;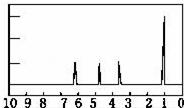 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
.