题目内容
7.下面是用98%的浓硫酸(ρ=1.84g/cm3)配制480mL 0.25mol/L稀硫酸的操作,请按要求填空:(1)所需浓硫酸的体积为6.8mL.(计算结果精确到小数点后一位)
(2)如果实验室有10mL、20mL、50mL量筒,应选用10mL量筒最好.将量取的浓硫酸沿烧杯内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌,目的是防止受热不均,液体飞溅.
(3)将冷却至室温的上述溶液沿玻璃棒注入500mL容量瓶中,并用50mL蒸馏水洗涤2-3次,洗涤液要注入到500mL容量瓶中,并摇匀.
(4)加蒸馏水至距刻度线下1-2cm处,改用胶头滴管滴加至液面与刻度线相切.
分析 (1)先计算出浓硫酸的物质的量浓度为c=$\frac{1000ρω}{M}$,然后根据溶液稀释定律C浓V浓=C稀V稀来计算;
(2)依据浓硫酸体积选择合适量筒;依据浓硫酸稀释操作解答;
(3)依据配制一定物质的量浓度溶液操作解答;
(4)依据定容的正确操作解答.
解答 解:(1)98%的浓硫酸(ρ=1.84g/cm3)物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,配制480mL 0.25mol/L稀硫酸,应选择500mL容量瓶,实际配制500mL溶液,依据溶液稀释定律C浓V浓=C稀V稀得:18.4mol/L×V=500mL×0.25mol/L,解得V=6.8mL;
故答案为:6.8mL;
(2)量取6.8mL浓硫酸,应选择10mL量筒,浓硫酸稀释的正确操作为:将量取的浓硫酸沿烧杯内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌,目的是防止受热不均,液体飞溅;
故答案为:10;烧杯;防止受热不均,液体飞溅;
(3)配制480mL 0.25mol/L稀硫酸,应选择500mL容量瓶,实际配制500mL溶液,操作步骤为:计算、量取、稀释、移液、洗涤、定容、摇匀等,将冷却至室温的上述溶液沿玻璃棒注入500mL容量瓶中,并用50mL蒸馏水洗涤2-3次,洗涤液要注入到500mL容量瓶中,并摇匀;
故答案为:玻璃棒;500mL容量瓶;洗涤2-3次;500mL容量瓶;
(4)定容时,加蒸馏水至距刻度线下1-2cm处,改用胶头滴管滴加至液面与刻度线相切,故答案为:1-2cm;胶头滴管;液面与刻度线相切.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,明确配制原理和操作步骤是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 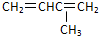 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. | CH3CH(OH)CH2CH32-羟基丁烷 | ||
| C. |  顺-2-丁烯 顺-2-丁烯 | D. | CH3CH(NH2)CH2COOH 3-氨基丁酸 |
15.下列有关物质性质或应用的说法正确的是( )
| A. | 钠的金属性比钾强,工业上用钠制取钾(Na+KCl $\frac{\underline{\;800℃\;}}{\;}$K↑+NaCl) | |
| B. | 利用Al2O3制作的坩埚,可用于熔融烧碱 | |
| C. | 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 | |
| D. | 制水泥和玻璃都用石灰石作原料 |
12.把下列四种 X 溶液,分别加入四个盛有 10mL 2mol/L 盐酸的烧杯中,均加水稀释到 50mL,此时 X 与盐酸和缓地进行反应.其中反应速率最大的是( )
| A. | 20mL3mol/L 的 X 溶液 | B. | 20mL2mol/L 的 X 溶液 | ||
| C. | 10mL4mol/L 的 X 溶液 | D. | 10mL2mol/L 的 X 溶液 |
19.下述有机物的变化中,属于消去反应的是( )
| A. | CH3CH2CH2OH+CuO $\stackrel{△}{→}$ CH3CH2CHO+H2O+Cu | |
| B. | CH3-C≡CH+HCl $\stackrel{催化剂}{→}$ CH3CCl=CH2 | |
| C. | CH3CH2CH2Cl+NaOH $→_{△}^{醇}$ CH3CH=CH2+NaCl+H2O | |
| D. | CH3CH2CH2Cl+NaOH$\stackrel{△}{→}$ CH3CH2CH2OH+NaCl |
16.下列基态原子的电子排布式或价电子排布式中,正确的是( )
| A. | Ca:1s22s22p63s23p63d2 | B. | Cu:3d94s2 | ||
| C. | Fe:3d64s2 | D. | C:1s22s12p3 |
17.下列反应的离子方程式书写正确的是( )
| A. | 硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| B. | 向石灰水中加入过量小办打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| C. | 向Ca(ClO)2中通放少量CO2:2ClO -+CO2+H2O=2HClO+CO32- | |
| D. | 用稀硝酸除去试管内壁的银镜:Ag+NO3-+2H+=Ag++NO2↑+H2O |