��Ŀ����
6�� �����ǵ����ʴ�л�IJ��Ҳ����Ҫ�Ļ�ѧ���ϣ���ҵ�ϳ����ط�Ӧ���£�
�����ǵ����ʴ�л�IJ��Ҳ����Ҫ�Ļ�ѧ���ϣ���ҵ�ϳ����ط�Ӧ���£�2NH3��g��+CO2��g���TCO��NH2��2��s��+H2O��g��
��1����һ����պ����ܱ������г���CO2��NH3����������Ӧ�ϳ����أ��㶨�¶��»�������еİ���������ͼ��ʾ��
A�������Ӧ����v����CO2����B����淴Ӧ����v����CO2�� �����������������=������
������ƽ��ת����Ϊ75%��
��2������������Ǻϳ����ص�һ���м����������Ϊ2��1��NH3��CO2����������һ���ݻ����������ܱ������У��ں㶨�¶���ʹ�䷢�����з�Ӧ���ﵽƽ�⣺2NH3��g��+CO2��g���TNH2COONH4��s��
��ʵ���õIJ�ͬ�¶��µ�ƽ�����������±���
| �¶ȣ��棩 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ��������Ũ�� ��10-3mol/L�� | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A����H��0����S��0B����H��0����S��0 C����H��0����S��0D����H��0����S��0
�ڹ���������Ӧ��ƽ��״̬����˵����ȷ����C
A������������İ�������泥���Ӧ���ת���ʽ�����
B��ƽ��ʱ������ϵ�¶ȣ�CO2����������½�
C��NH3��ת����ʼ�յ���CO2��ת����
D��������Ч�Ĵ����ܹ���߰�������淋IJ���
��3����ѧ�������о����ض���ȼ�ϵ�أ���ҺҲ�ܷ��磡�����ֵ��ֱ��ȥ�����з�ˮ�е����أ����ܲ���������ˮ���ܷ��磮����ȼ�ϵ�ؽṹ��ͼ��ʾ��д���õ�صĸ�����Ӧʽ��CO��NH2��2+H2O-6e-=CO2+N2+6H+��

���� ��1����ͼ��֪����ʼʱ�������������Ϊ50%��60s�ﵽƽ��״̬�����������СΪ20%��A��ʱ��Ӧ�����ƶ�����
2NH3��g��+CO2��g���TCO��NH2��2��s��+H2O��g��
��ʼ a a 0
ת�� 2x x x
ƽ�� a-2x a-x x
��$\frac{a-2x}{2a-2x-x+x}$��100%=20%�����x=$\frac{3}{8}$a���Դ˼���ת���ʣ�
��2����2NH3��g��+CO2��g���TNH2COONH4��s���������С���ɱ������ݿ�֪���¶�Խ�ߣ�ƽ��������Ũ��Խ���������¶�ƽ�������ƶ���
��A������������İ�������泥�ƽ�ⲻ�ƶ���
B��ƽ��ʱ�����¶ȣ�ƽ�������ƶ�����CO2������������䣻
C���������Ϊ2��1��NH3��CO2������壬ת����Ϊ2��1��
D��������Ч�Ĵ�����ƽ�ⲻ�ƶ���
��3��������ȼ�ϵ�صĽṹ��֪�������������õ���������ˮ������������ʧȥ�������ɵ����Ͷ�����̼��
��� �⣺��1����ͼ��֪����ʼʱ�������������Ϊ50%��60s�ﵽƽ��״̬�����������СΪ20%��A��ʱ��Ӧ�����ƶ�����֪A�������Ӧ����v����CO2����B����淴Ӧ����v����CO2������
2NH3��g��+CO2��g���TCO��NH2��2��s��+H2O��g��
��ʼ a a 0
ת�� 2x x x
ƽ�� a-2x a-x x
��$\frac{a-2x}{2a-2x-x+x}$��100%=20%�����x=$\frac{3}{8}$a��
������ƽ��ת����Ϊ$\frac{\frac{3}{8}a��2}{a}$��100%=75%��
�ʴ�Ϊ������75%��
��2����2NH3��g��+CO2��g���TNH2COONH4��s���������С�����S��0���ɱ������ݿ�֪���¶�Խ�ߣ�ƽ��������Ũ��Խ���������¶�ƽ�������ƶ�����֪����ӦΪ���ȷ�Ӧ�����H��0���ʴ�Ϊ��A��
��A������������İ�������泥�ƽ�ⲻ�ƶ�����Ӧ���ת���ʲ��䣬��A����
B��ƽ��ʱ�����¶ȣ�ƽ�������ƶ�����CO2������������䣬��B����
C���������Ϊ2��1��NH3��CO2������壬ת����Ϊ2��1����NH3��ת����ʼ�յ���CO2��ת���ʣ���C��ȷ��
D��������Ч�Ĵ�����ƽ�ⲻ�ƶ�����������淋IJ��ʲ��䣬��D����
�ʴ�Ϊ��C��
��3��������ȼ�ϵ�صĽṹ��֪������������ʧȥ�������ɵ����Ͷ�����̼��������ӦΪCO��NH2��2+H2O-6e-=CO2+N2+6H+���ʴ�Ϊ��CO��NH2��2+H2O-6e-=CO2+N2+6H+��
���� ���⿼�黯ѧƽ����㼰ԭ��ء��ʱ�ȣ�Ϊ��Ƶ���㣬���ջ�ѧƽ�����η���ת���ʵļ��㡢�缫��ӦΪ���Ĺؼ������ط�������������Ŀ��飬ע��ƽ���ƶ�ԭ����Ӧ�ã���Ŀ�Ѷ��еȣ�

| A�� | pH=1����Һ�У�K+��Fe2+��NO${\;}_{3}^{-}$��Cl- | |
| B�� | 0.1 mol•L-1NaHCO3��Һ��Na+��Ba2+��NO${\;}_{3}^{-}$��OH- | |
| C�� | �μ�KSCN��Һ�Ժ�ɫ����Һ��NH${\;}_{4}^{+}$��K+��Cl-��I- | |
| D�� | ����������Һ�У�Cu2+��K+��SO${\;}_{4}^{2-}$��Cl- |
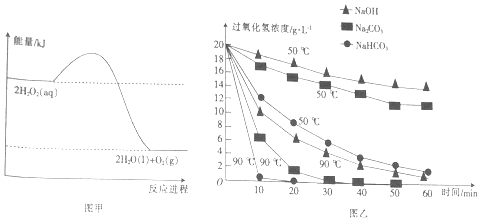
| A�� | H2O2�ķֽⷴӦΪ���ȷ�Ӧ | |
| B�� | ���ѹ��ۼ������������2��E��O-O����1��E��O=O�� | |
| C�� | ������ͬ����ʱ���¶�Խ�ߣ�H2O2�ֽ������Խ�� | |
| D�� | ��ͬ�¶��£����벻ͬ���ʵ���Һ������Խǿ��H2O2�ֽ������Խ�� |
| A�� | 101kPaʱ��2H2��g��+O2��g���T2H2O��g������H=-QkJ•mol-1����H2��ȼ����Ϊ$\frac{1}{2}$QkJ•mol-1 | |
| B�� | ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ | |
| C�� | 500�桢30MPa�£���0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ�� N2��g��+3H2��g��$?_{500�棬30MPa}^{����}$2NH3��g����H=-38.6kJ•mol-1 | |
| D�� | H+��aq��+OH-��aq���TH2O��l������H=-57.3kJ•mol-1����1mol NaOH������������Һ�뺬0.5mol H2SO4��Ũ�����Ϻ�ų�57.3kJ������ |
��1���������ƣ�Na2FeO4����ˮ���������е�һ�����;�ˮ�������������Աȸ�����ظ�ǿ�������ڷ�Ӧ�б���ԭ�����������Ӵﵽ��ˮ��Ŀ�ģ���Ҫ��ش��������⣺
����������Ҫͨ�����·�Ӧ��ȡ��2Fe��OH��3+3NaClO+4NaOH�T2Na2FeO4+3X+5H2O����X�Ļ�ѧʽNaCl����Ӧ��Fe��������
��2�������������ϸ�ijЩ���ϻ�ϣ������Ƴɷ������ᣮ�Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȣ����������Ʊ����죨Fe2O3���Ĺ�����ͼ��
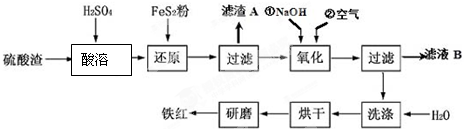
�����ܹ�����Fe2O3��ϡ���ᷴӦ�Ļ�ѧ����ʽΪFe2O3+3H2SO4�TFe2��SO4��3+3H2O��
������A����Ҫ�ɷݵĻ�ѧʽΪSiO2��
�ڻ�ԭ�����м���FeS2��Ŀ���ǽ���Һ�е�Fe3+��ԭΪFe2+��������������ΪH2SO4������ɸ÷�Ӧ�����ӷ���ʽ��FeS2+14Fe3++8H2O�T15Fe2++2SO42-+16H+��
�����������У�O2��NaOH��Fe2+��Ӧ�����ӷ���ʽΪ4Fe2++O2+2H2O+8OH-=4Fe��OH��3����
| ������ | Fe��OH��3 | Al��OH��3 | Fe��OH��2 | Mg��OH��2 |
| ��ʼ����pH | 2.7 | 3.8 | 7.6 | 9.4 |
| ��ȫ����pH | 3.2 | 5.2 | 9.7 | 12.4 |
| ������ | Fe��OH��3 | Al��OH��3 | Fe��OH��3 | Mg��OH��2 |
| ��ʼ����Ph | 2.7 | 3.8 | 7.6 | 9.4 |
| ��ȫ����pH | 3.2 | 5.2 | 9.7 | 12.4 |
 �������ȣ�ClNO�����л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO��g��+Cl2��g��?2ClNO��g����
�������ȣ�ClNO�����л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO��g��+Cl2��g��?2ClNO��g������1����2NO2��g��+NaCl��s��?NaNO3��s��+ClNO��g�� K1
��4NO2��g��+2NaCl��s��?2NaNO3��s��+2NO��g��+Cl2��g�� K2
��2NO��g��+Cl2��g��?2ClNO��g�� K3
��K1��K2��K3֮��Ĺ�ϵΪ$\frac{{{K}^{2}}_{1}}{{K}_{2}}$��
��2����֪���ֻ�ѧ���ļ����������±����������ȵĽṹΪCl-N=O����
| ��ѧ�� | N=O | Cl-Cl | Cl-N | N-O |
| ����/��kJ•mol-1�� | 630 | 243 | a | 607 |
��3��300��ʱ��2NO��g��+Cl2��g��?2ClNO��g��������Ӧ���ʱ���ʽΪv��=k•cn��ClNO����������ʺ�Ũ�ȵĹ�ϵ���±���
| ��� | c��ClNO��/mol•L-1 | v/mol•L-1•s-1 |
| �� | 0.30 | 3.6��10-8 |
| �� | 0.60 | 1.44��10-8 |
| �� | 0.90 | 3.24��10-8 |
��4����1L�ĺ����ܱ������г���2molNO��g����1molCl2��g�����ڲ�ͬ�¶��²��c��ClNO����ʱ��Ĺ�ϵ
��ͼA��
�ٸ÷�Ӧ�ġ�H��0���������������=������
�ڷ�Ӧ��ʼ��10minʱNO��ƽ����Ӧ����v��NO��=0.1mol•L-1•min-1
��T2ʱ�÷�Ӧ��ƽ�ⳣ��K=2��
��5��һ���������ں��º��ݵ��ܱ������а�һ����������NO��g����Cl2��g����ƽ��ʱClNO�����������$\frac{n��NO��}{n��C{l}_{2}��}$�ı仯ͼ����ͼB����A��B��C��״̬�У�NO��ת����������A�㣬��$\frac{n��NO��}{n��C{l}_{2}��}$=1.5ʱ���ﵽƽ��״̬ClNO���������������D��E��F�����е�D�㣮
��֪���йؽ��������γ������������ʱ��pH�����
| ��ʼ����ʱ��pH | ��ȫ����ʱ��pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
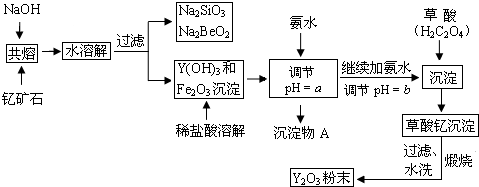
��1���ƿ�ʯ��Y2FeBe2Si2O10������������������ʽ�ɱ�ʾΪY2O3•FeO•2BeO•2SiO2��
��2������Na2SiO3��Na2BeO2�Ļ����Һ���Ƶ�Be��OH��2��������
�����ѡ�����ᡢb������ĸ�������Լ�����ͨ����Ҫ�IJ�������ʵ�֣�
a��NaOH��Һ b����ˮ c��CO2�� d��HNO3
��д��Na2BeO2���������ᷢ����Ӧ�����ӷ���ʽ��BeO22-+4H+=Be2++2H2O��
��3��ΪʹFe3+������ȫ�����ð�ˮ����pH=a����aӦ������3.7��a��6.0�ķ�Χ�ڣ�����Fe3+�Ƿ������ȫ�IJ���������ȡ������Һ���μӼ���KSCN��Һ���۲���Һ�Ƿ��ΪѪ��ɫ��������Ѫ��ɫ����˵��Fe3+��ȫ��������֮��δ��ȫ������
| A�� | ֬�� | B�� | �� | C�� | ���� | D�� | ������ |
| A�� | �� Ba��OH��2��Һ�������������� | |
| B�� | ��Ba��OH��2��Һ�����������������ټ����ᣬ�����ܽ⣬ͬʱ�������� | |
| C�� | ��Ba��OH��2��Һ�����������������ټ����ᣬ�����ܽ⣬ͬʱ������ɫ��ζ��ʹ����ʯ��ˮ����ǵ����� | |
| D�� | ��BaCl2��Һ��û�г������ټ�NaOH��Һ�����������������������ᣬ�����ܽ⣬ͬʱ������ɫ��ζ��ʹ����ʯ��ˮ����ǵ����� |