题目内容
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO) 共5.92g,经如图处理:

下列说法正确的是( )
①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中含氧元素的物质的量为0.03mol
③溶解样品的过程中消耗硫酸的总物质的量为0.04mol
④V=224mL
⑤V=336mL.

下列说法正确的是( )
①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中含氧元素的物质的量为0.03mol
③溶解样品的过程中消耗硫酸的总物质的量为0.04mol
④V=224mL
⑤V=336mL.
| A、①③④ | B、②③④ |
| C、②③⑤ | D、①③⑤ |
考点:有关混合物反应的计算,铁的氧化物和氢氧化物,铜金属及其重要化合物的主要性质
专题:计算题
分析:①金属铁、氧化铁、氧化铜可以和硫酸反应,金属铜可以和三价铁反应;
②根氧化铁的量和元素守恒来确定铁元素的物质的量、质量,再根据样品总质量、铜、铁元素的质量计算出氧元素的质量、物质的量;
③铁与足量稀硫酸反应生成硫酸亚铁,根据铁元素的物质的量计算出消耗硫酸的物质的量;
④根据药品中铁元素、氧元素的物质的量及消耗硫酸的物质的量计算出生成氢气的氢离子的物质的量,再根据质量守恒计算出生成氢气的物质的量及标况下的体积;
⑤根据④的计算结果进行判断.
②根氧化铁的量和元素守恒来确定铁元素的物质的量、质量,再根据样品总质量、铜、铁元素的质量计算出氧元素的质量、物质的量;
③铁与足量稀硫酸反应生成硫酸亚铁,根据铁元素的物质的量计算出消耗硫酸的物质的量;
④根据药品中铁元素、氧元素的物质的量及消耗硫酸的物质的量计算出生成氢气的氢离子的物质的量,再根据质量守恒计算出生成氢气的物质的量及标况下的体积;
⑤根据④的计算结果进行判断.
解答:
解:①铜不与稀硫酸反应,则生成的滤渣3.2g为铜,金属铜可以和三价铁反应,所以滤液A中一定不含有+3价铁离子,故①错误;
②最后加热得到的3.2g固体为三氧化二铁,其物质的量为:
=0.02mol,Fe元素的物质的量为:n(Fe)=0.02mol×2=0.04mol,铁元素的质量为:0.04mol×56g/mol=2.24g,则样品中氧元素的质量为:5.92g-2.24g-3.2g=0.48g,氧元素的物质的量为:
=0.03mol,故②正确;
③根据②铁元素的物质的量为0.04mol,铁与过量稀硫酸反应生成硫酸亚铁,则反应消耗硫酸的物质的量为0.04mol,故④正确;
④最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,含氢离子0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,根据②可知氧元素的物质的量为0.03mol,它结合氢离子0.06mol,所以硫酸中生成氢气的氢离子为:0.08mol-0.06mol=0.02mol,即生成0.01mol氢气,标况体积为0.01mol氢气的体积为2.24L,故④正确;
⑤根据④的计算可知,生成标况下氢气的体积为2.24L,故⑤错误;
根据以上分析可知,正确的为②③④,
故选B.
②最后加热得到的3.2g固体为三氧化二铁,其物质的量为:
| 3.2g |
| 160g/mol |
| 0.48g |
| 16g/mol |
③根据②铁元素的物质的量为0.04mol,铁与过量稀硫酸反应生成硫酸亚铁,则反应消耗硫酸的物质的量为0.04mol,故④正确;
④最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,含氢离子0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,根据②可知氧元素的物质的量为0.03mol,它结合氢离子0.06mol,所以硫酸中生成氢气的氢离子为:0.08mol-0.06mol=0.02mol,即生成0.01mol氢气,标况体积为0.01mol氢气的体积为2.24L,故④正确;
⑤根据④的计算可知,生成标况下氢气的体积为2.24L,故⑤错误;
根据以上分析可知,正确的为②③④,
故选B.
点评:本题考查了元素以及化合物性质、有关混合物的计算,题目难度中等,注意掌握常见金属单质及其化合物的性质,明确反应流程中的反应原理及组成为解答本题的关键.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
能正确表示下列反应的离子方程式是( )
| A、硫酸铝溶液中加入过量氨水Al3++3OH-═Al(OH)3↓ | ||||
| B、向水中通入氯气:Cl2+H2O=2H++Cl-+ClO- | ||||
C、MnO2与浓盐酸共热制Cl2:MnO2+4H++2Cl-
| ||||
| D、向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O |
化学与人类生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺的状况 |
| B、大量使用化肥和农药,以提高农作物产量 |
| C、含磷化合物的排放是“水华”和“赤潮”产生的原因 |
| D、安装煤炭“固硫”装置,降低酸雨发生率 |
有两种金属组成的混合物粉末15g与足量的稀盐酸反应,生成11.2L(标况)H2,则该混合物的组成可能是( )
| A、Fe、Zn |
| B、Al、Cu |
| C、Al、Mg |
| D、Al、Fe |
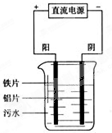 电浮选凝聚法是工业上采用的一种污水处理方法如图是电解污水装置示意图.
电浮选凝聚法是工业上采用的一种污水处理方法如图是电解污水装置示意图. HClamol
HClamol Na2CO3bmol
Na2CO3bmol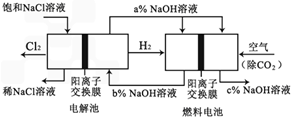
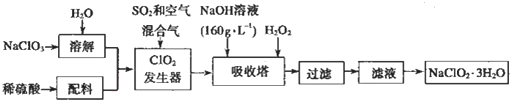
 次氯酸钠(NaClO)和藏氯酸钠(NaClO)都是重要的含氯消毒剂.
次氯酸钠(NaClO)和藏氯酸钠(NaClO)都是重要的含氯消毒剂.