题目内容
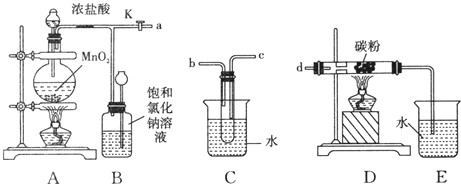
10.实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:负极:Pb+SO42--2e-═PbSO4
正极:PbO2+4H++SO42-+2e-═PbSO4+2H2O
今欲制得Cl2 0.050mol,这时电池内消耗的H2SO4的物质的量至少是( )
| A. | 0.025 mol | B. | 0.050 mol | C. | 0.100 mol | D. | 0.200 mol |
分析 根据反应2Cl--2e-=Cl2↑计算出生成0.050mol氯气转移电子的物质的量,然后根据反应PbO2+Pb+2H2SO4=2PbSO4+2H2O计算出至少消耗硫酸的物质的量.
解答 解:根据反应2Cl--2e-=Cl2↑可知,生成0.050mol氯气失去电子的物质的量为:0.050mol×2=0.0100mol,
设消耗硫酸的物质的量为ymol,则:
PbO2+Pb+2H2SO4=2PbSO4+2H2O 转移电子
2mol 2mol
y 0.100mol
解:y=0.100,
所以生成0.050mol氯气消耗硫酸的物质的量至少为0.100mol,
故选C.
点评 本题考查了电解原理及其应用,题目难度中等,明确电解原理为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
1.下列实验操作中正确的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| C. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴 | |
| D. | 蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸 |
18.下列离子方程式书写正确的是( )
| A. | 向NaHCO3溶液中加入足量的Ba(OH)2溶液2HCO3-+Ba2++2OH-═BaCO3↓+CO32-+2H2O | |
| B. | 向石灰石中滴加稀硝酸CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 用惰性电极电解KOH溶液时阴极电极反应2H2O-4e-═O2+4H+ | |
| D. | NaOH溶液中通入少量硫化氢气体:2OH-+H2S═S2-+2H2O |
5.A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如图所示,其中Z元素原子最外层电子数是电子层数的2倍.请回答下列问题:
(1)W的最高价氧化物化学式是Cl2O7;Z 的原子结构示意图为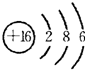 .
.
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂
c.将 X的简单气态氢化物及时移离 d.增大反应体系的压强
(5)标准状况下,2.24 L X的简单气态氢化物被200 mL 1 mol•L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-).
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用 WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
| X | Y | |
| Z | W |
 .
.(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O.
(3)AW3可用于净水,其原理是Al3++3H2O?Al(OH)3(胶体)+3H+.(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应.下列措施中既能提高反应速率,又能提高原料转化率的是d.
a.升高温度 b.加入催化剂
c.将 X的简单气态氢化物及时移离 d.增大反应体系的压强
(5)标准状况下,2.24 L X的简单气态氢化物被200 mL 1 mol•L-1 X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)c(NO3-)>c(H+)>c(NH4+)>c(OH-).
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用 WY2(沸点9.9℃)氧化除去CN-的离子方程式2ClO2+2CN-═N2+2CO2+2Cl-.
15.下列溶液中导电性最强的是( )
| A. | 1L 0.1mol/L醋酸 | B. | 1L 0.1mol/L硫酸 | ||
| C. | 0.5L0.1mol/L盐酸 | D. | 2L0.1moL/L的磷酸 |
19.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下:
(1)铜帽溶解时加入H2O2 的目的是Cu+H2O2+H2SO4=CuSO4+2H2O(用化学方程式表示).铜帽溶解完全后,需将溶液中过量的H2O2 除去.除去H2O2 的简便方法是加热至沸.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的浓度.实验操作为:准确量取100mL含有Cu2+的溶液于烧杯中,取溶液20mL加水稀释至100mL,调节溶液pH=3~4,加入过量的KI,用0.1mol/L Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2 2S2O32-+I2═2I-+S4O62-
①滴定选用的指示剂为淀粉溶液
②若滴定前溶液中的H2O2 没有除尽,所测定的Cu2+含量将会偏高(填“偏高”、“偏低”或“不变”).
③若滴定中消耗Na2S2O3标准溶液25mL,则原溶液中Cu2+物质的量浓度为0.125mol/L.
(3)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成ZnO22-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30%H2O2、1.0mol•L-1HNO3、1.0mol•L-1NaOH.
由除去铜的滤液制备ZnO 的实验步骤依次为:
①向滤液中加入30%H2O2,使其充分反应;②滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;③过滤;④向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全;⑤过滤、洗涤、干燥;⑥900℃煅烧.

(1)铜帽溶解时加入H2O2 的目的是Cu+H2O2+H2SO4=CuSO4+2H2O(用化学方程式表示).铜帽溶解完全后,需将溶液中过量的H2O2 除去.除去H2O2 的简便方法是加热至沸.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的浓度.实验操作为:准确量取100mL含有Cu2+的溶液于烧杯中,取溶液20mL加水稀释至100mL,调节溶液pH=3~4,加入过量的KI,用0.1mol/L Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2 2S2O32-+I2═2I-+S4O62-
①滴定选用的指示剂为淀粉溶液
②若滴定前溶液中的H2O2 没有除尽,所测定的Cu2+含量将会偏高(填“偏高”、“偏低”或“不变”).
③若滴定中消耗Na2S2O3标准溶液25mL,则原溶液中Cu2+物质的量浓度为0.125mol/L.
(3)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成ZnO22-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L-1计算).
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
由除去铜的滤液制备ZnO 的实验步骤依次为:
①向滤液中加入30%H2O2,使其充分反应;②滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;③过滤;④向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全;⑤过滤、洗涤、干燥;⑥900℃煅烧.
20.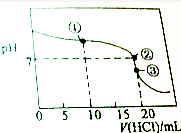 常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
 常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )
常温下,用0.1000mol•L-1的盐酸滴定20.00mL未知浓度的氨水,滴定曲线如图所示,滴加20.00mL盐酸时所得溶液中,c(Cl-)=c(NH4+)+c(NH3•H2O)+c(NH3),下列说法错误的是( )| A. | 该氨水的浓度0.1000mol•L-1 | |
| B. | 点①溶液中c(NH4+)+c(NH3•H2O)+c(NH3)=2c(Cl-) | |
| C. | 点②溶液中c(NH4+)=c(Cl-) | |
| D. | 点③溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-) |