题目内容
6.下列关于钠元素的几种表达式错误的是( )| A. | Na+的电子排布图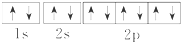 | |
| B. | Na+的结构示意图: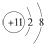 | |
| C. | 基态Na原子的电子排布式:1s22s22p53s2 | |
| D. | 基态Na原子的价电子排布式:3s1 |
分析 A、钠离子的核电荷数为11,核外电子数为10,核外电子排布式为1s22s22p6;
B、Na+的原子核内有11个质子,核外有10个电子,结构示意图为 ;
;
C、基态Na原子的电子排布式::1s22s22p63s1;
D、基态Na原子的价电子就是最外层电子,所以基态Na原子的价电子排布式:3s1.
解答 解:A、钠离子的核电荷数为11,核外电子数为10,核外电子排布式为1s22s22p6,电子排布图: ,故A不选;
,故A不选;
B、Na+的原子核内有11个质子,核外有10个电子,结构示意图为 ,故B不选;
,故B不选;
C、基态Na原子的电子排布式::1s22s22p63s1,故C选;
D、基态Na原子的价电子就是最外层电子,所以基态Na原子的价电子排布式:3s1,故D不选;
故选C.
点评 本题考查原子核外电子排布,为高考常见题型,难度不大,注意把握原子核外电子的排布规律,把握电子排布式和轨道式的书写方法.

练习册系列答案
相关题目
17.下列有机物的命名正确的是( )
| A. |  2-甲基-3-丁烯 | B. |  乙 基苯 | C. |  2-乙基 丙烷 | D. |  1-甲基乙醇 |
14.下列各组物质性质的比较中,错误的是( )
| A. | 还原性:HF<HCl<H2S | B. | 金属性:Na>Mg>Be | ||
| C. | 非金属性:F>Cl>S | D. | 离子半径:Al3+>Mg2+>F- |
1.离子键、共价键、金属键、范德华力都是微粒之间的不同作用力,下列物质:①Na2O2 ②SiO2 ③氦气 ④金刚石 ⑤NH4Cl ⑥白磷 含有上述任意两种作用力的是( )
| A. | ①②④ | B. | ①③⑥ | C. | ①⑤⑥ | D. | ③④⑤ |
15.下列离子方程式的书写正确的是( )
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | NaHCO3溶液与NaOH溶液反应:2OH-+2HCO3-═2 CO32-+H2O | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 钠和冷水反应 2Na+2H2O═2Na++2OH-+H2↑ |
16.已知反应:Cl-+ClO-+2H+=Cl2↑+H2O,下列说法正确的是( )
| A. | Cl-、ClO-在酸性溶液中不能大量共存 | |
| B. | 在无色碱性溶液中:ClO、Cl-、Fe2+、Na+能大量共存 | |
| C. | 洁厕灵(主要成分是盐酸)和84消毒液(主要成分是次氯酸钠)混合使用效果更好 | |
| D. | 符合该离子方程式的化学方程式可以是:HClO+HCl=Cl2↑+H2O |
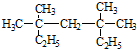 系统命名法为3,3,5,5-四甲基庚烷,
系统命名法为3,3,5,5-四甲基庚烷, ,
,