题目内容
9.某同学用某种粗盐进行提纯实验,步骤见图.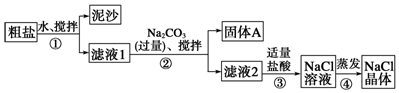
请回答下列问题:
(1)步骤①和②的操作名称是过滤.
(2)步骤③判断加入盐酸“适量”的方法是滴加盐酸至无气泡产生为止;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止溶液飞溅,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | Ⅰ有气泡放出,澄清石灰水变浑浊 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入Ⅱ稀硝酸,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | Ⅲ猜想Ⅱ不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,Ⅳ滴入BaCl2溶液和稀HNO3溶液 | Ⅴ有白色沉淀且不溶于稀HNO3 | 猜想Ⅲ成立 |
分析 由流程可知,粗盐溶解后过滤得到泥沙,滤液1中加过量碳酸钠可除去钙离子,固体A为碳酸钙,滤液2中含氯化钠、碳酸钠,加盐酸与碳酸钠反应,然后蒸发得到NaCl,
(1)步骤①②均为分离不溶性固体与溶液;
(2)滴定盐酸无气泡可知碳酸钠除尽;步骤④加热蒸发时要用玻璃棒不断搅拌,防止局部温度过高,液滴飞溅;
(3)碳酸盐与盐酸反应生成二氧化碳气体;
碳酸盐溶于硝酸,钡离子与硫酸根离子结合生成硫酸钡白色沉淀;
硫酸盐与氯化钡反应生成不溶于硝酸的硫酸钡沉淀,以此来解答.
解答 解:(1)步骤①②均为分离不溶性固体与溶液,操作名称均为过滤,故答案为:过滤;
(2)步骤③判断加入盐酸“适量”的方法是滴加盐酸至无气泡产生为止;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止溶液飞溅,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干,
故答案为:滴加盐酸至无气泡产生为止;溶液飞溅;
(3)取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口,观察到有气泡放出,澄清石灰水变浑浊,则猜想I成立;
取少量固体A于试管中,先滴入Ⅱ稀硝酸,再滴入Na2SO4溶液,观察到有气泡放出,无白色沉淀,则猜想Ⅱ不成立;
取少量NaCl晶体溶于试管中的蒸馏水,Ⅳ滴入BaCl2溶液和稀HNO3溶液,观察到有白色沉淀且不溶于稀HNO3,则猜想Ⅲ成立,
故答案为:有气泡放出,澄清石灰水变浑浊;稀硝酸; 猜想Ⅱ不成立;滴入BaCl2溶液和稀HNO3溶液;有白色沉淀且不溶于稀HNO3.
点评 本题考查粗盐提纯,为高频考点,把握流程中粗盐提纯的试剂、发生的反应及混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意物质检验与离子检验的方法相结合,题目难度不大.

练习册系列答案
相关题目
20.某溶液中只可能含有下列离子中的几种:K+、NO3-、SO42-、NH4+、CO32-(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
下列说法正确的是( )
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.
下列说法正确的是( )
| A. | 该溶液中一定不含NO3- | |
| B. | 该溶液中一定含K+,且c(K+)≥0.1mol/L | |
| C. | 该溶液中可能含K+ | |
| D. | 该溶液中肯定含有NO3?、SO42-、NH4+、CO32- |
17.某有机物的结构简式为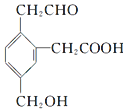 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦缩聚.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦缩聚.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤⑦ | D. | ②③④⑤⑥ |
4.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,1.01×105Pa,11.2L Cl2含有的分子数小于0.5NA | |
| B. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA | |
| C. | 1molFeCl3与沸水反应生成NA个Fe(OH)3胶粒 | |
| D. | 常温下,23 g NO2含有2NA个氧原子 |
14.标准状况下,质量相等的下列物质中体积最大的是( )
| A. | N2 | B. | Cl2 | C. | H2 | D. | CO2 |
1.下列各项与化学平衡移动原理无关的是( )
| A. | 加催化剂,使N2和H2在一定的条件下转化为NH3 | |
| B. | 收集氯气用排饱和食盐水的方法 | |
| C. | 加压条件下有利于SO2和O2反应生成SO3 | |
| D. | 可用浓氨水和氢氧化钠固体快速制取氨气 |
18.无机化合物可根据其组成和性质进行分类,
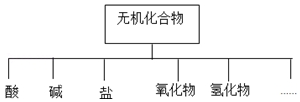
(1)如图所示的物质分类方法名称是树状分类法.
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑩后面.
(3)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学反应方程式为:SO2+2NaOH=Na2SO3+H2O.
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于正盐盐(填正盐、酸式盐或碱式盐).

(1)如图所示的物质分类方法名称是树状分类法.
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑩后面.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①H2SO4 ② | ③NaOH ④ | ⑤Na2SO4 ⑥ | ⑦SO2 ⑧ | ⑨NH3 ⑩ |
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于正盐盐(填正盐、酸式盐或碱式盐).
19.下列不属于自发进行的变化是( )
| A. | 红墨水加到清水使整杯水变红 | B. | 冰在室温下融化成水 | ||
| C. | 铁器在潮湿的空气中生锈 | D. | 电解饱和食盐水 |