题目内容
14.下列数量的物质中含对应微粒数目最多的是( )| A. | 0.8molNaCl所含离子数 | B. | 标准状况下5.6L CO2所含原子数 | ||
| C. | 1L1 mol•L-1盐酸溶液所含H原子数 | D. | 10g氖气所含原子数 |
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$结合物质的构成计算.
解答 解:A.0.8molNaCl含有1.6mol离子;
B.标准状况下5.6L CO2所含原子的物质的量为$\frac{5.6L}{22.4L/mol}$×3=0.75mol;
C.盐酸中含有水,含有的H原子数约为n(HCl)+2n(H2O)=1mol+$\frac{1000g}{18g/mol}$×2=112mol;
D.10g氖气所含原子数为$\frac{10g}{20g/mol}$=0.5mol,
则含有的微粒数最多的为C.
故选C.
点评 本题考查物质的量的相关计算,为高频考点,侧重学生的分析、计算能力的考查,注意把握物质的构成特点,难度不大,易错点为C,注意不能忽略水.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
4. 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.
(1)已知合成氨的反应是一个典型的可逆反应,在一个一定容积的密闭容器中加入1mol 氮气和3mol 氢气,在一定条件下发生反应合成氨气,当反应物转化率达10%时,测得放出的热量为9.24kJ,请写出该条件下合成氨反应的热化学方式: N2(g)+3H2( g)═2NH3(g)△H=-92.4 kJ•mol-1 .
(2)CO对合成氨的催化剂有毒害作用,常用乙酸二氨合铜(Ⅰ)溶液来吸收原料气中CO,其反应原理为
[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l)△H<0
通过下列哪种措施可提高CO的吸收效率A(填字母)
A.高压 B.高温 C.把[Cu(NH3)3]CH3COO•CO分离出去 D.增大CO浓度
吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是B.(填字母)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
(3)用氨气制取尿素[CO(NH2)2]的反应为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)△H<0
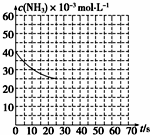
某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%.该温度下此反应平衡常数K的值为2500.图中的曲线表示该反应在前25s内的反应进程中的NH3浓度变化.若反应延续至70s,保持其他条件不变情况下,请在图中用实线画出使用催化剂时该反应的进程曲线.
(4)将尿素施入土壤后,大部分是通过转化为碳酸铵或碳酸氢铵后才被作物所利用,尿素分子在微生物分泌的脲酶作用下,转化为碳酸铵.已知弱电解质在水中的电离平衡常数(25℃)如下表:
现有常温下0.1mol•L-1的(NH4)2CO3溶液,
①你认为该溶液呈碱(填“酸”、“中”或“碱”性),原因是由于NH3•H2O的电离平衡常数大于HCO3-的电离平衡常数,因此CO32-水解程度大于NH4+水解程度,溶液中c (OH-)>c(H+),溶液呈碱性.
②就该溶液中粒子之间有下列关系式,你认为其中不正确的是B.
A.c(NH4+)>c(CO32-)>c(OH-)>c(H+)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D.c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.(1)已知合成氨的反应是一个典型的可逆反应,在一个一定容积的密闭容器中加入1mol 氮气和3mol 氢气,在一定条件下发生反应合成氨气,当反应物转化率达10%时,测得放出的热量为9.24kJ,请写出该条件下合成氨反应的热化学方式: N2(g)+3H2( g)═2NH3(g)△H=-92.4 kJ•mol-1 .
(2)CO对合成氨的催化剂有毒害作用,常用乙酸二氨合铜(Ⅰ)溶液来吸收原料气中CO,其反应原理为
[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l)△H<0
通过下列哪种措施可提高CO的吸收效率A(填字母)
A.高压 B.高温 C.把[Cu(NH3)3]CH3COO•CO分离出去 D.增大CO浓度
吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,再生的适宜条件是B.(填字母)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
(3)用氨气制取尿素[CO(NH2)2]的反应为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)△H<0
某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%.该温度下此反应平衡常数K的值为2500.图中的曲线表示该反应在前25s内的反应进程中的NH3浓度变化.若反应延续至70s,保持其他条件不变情况下,请在图中用实线画出使用催化剂时该反应的进程曲线.
(4)将尿素施入土壤后,大部分是通过转化为碳酸铵或碳酸氢铵后才被作物所利用,尿素分子在微生物分泌的脲酶作用下,转化为碳酸铵.已知弱电解质在水中的电离平衡常数(25℃)如下表:
| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 | 1.77×10-5 |
| Ka2=5.61×10-11 |
①你认为该溶液呈碱(填“酸”、“中”或“碱”性),原因是由于NH3•H2O的电离平衡常数大于HCO3-的电离平衡常数,因此CO32-水解程度大于NH4+水解程度,溶液中c (OH-)>c(H+),溶液呈碱性.
②就该溶液中粒子之间有下列关系式,你认为其中不正确的是B.
A.c(NH4+)>c(CO32-)>c(OH-)>c(H+)
B.c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1
D.c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
5.下列解释事实的方程式正确的是( )
| A. | 用已知浓度的NaOH溶液测定未知浓度的醋酸溶液的浓度:H++OH-═H2O | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2Na++2OH-═Na2SiO3+H2O | |
| C. | 利用铝热反应焊接钢轨:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| D. | 用氯水除去FeCl2溶液中的Fe2+:Cl2+Fe2+═2Cl-+Fe3+ |
2.下列叙述的方法不正确的是( )
| A. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| B. | 在铁板表面涂抹油漆,不能防止铁板被腐蚀 | |
| C. | 钢铁在干燥空气中不易被腐蚀 | |
| D. | 用牺牲锌块的方法来保护船身 |
9.实验室中需要配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四种离子的物质的量浓度均为1mol•L-1.下面四个选项中能达到此目的是( )
| A. | Na+、Cl-、SO42-、K+ | B. | K+、Cu2+、SO42-、NO3- | ||
| C. | K+、H+、HCO3-、Cl- | D. | Mg2+、Cl-、SO42-、Na+ |
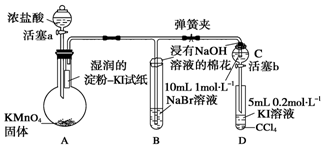
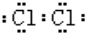 ;A中发生的反应的化学反应方程式为2KMnO4+16HCl═5Cl2↑+2MnCl2+2KCl+8H2O.
;A中发生的反应的化学反应方程式为2KMnO4+16HCl═5Cl2↑+2MnCl2+2KCl+8H2O.